题目内容
7.将三种黑色粉末组成的混合物加入到足量的某热浓酸中,充分反应后得到蓝绿色溶液和两种气体,将从蓝绿色溶液中分离得到的盐与0.15mol还原铁粉恰好反应完全,可得浅绿色溶液和6.4g红色沉淀;将上述生成的两种气体通入足量饱和NaHCO3溶液中,仍然收集到两种气体,据此推断黑色粉末可能为( )| A. | 物质的量 FeS:CuO:Fe=1:1:1 | B. | 物质的量 C:CuO:Fe=3:2:2 | ||
| C. | 质量 MnO2:CuO:C=5.5:8:12 | D. | 质量 Fe:C:CuO=7:5:3 |
分析 6.4g红色沉淀为Cu,其物质的量为:$\frac{6.4g}{64g/mol}$=0.1mol,根据反应Fe+Cu2+=Fe2++Cu可知,生成0.1mol铜需要消耗0.1mol还原铁粉,而实际上消耗了0.15mol铁粉,则反应后的溶液中除了含有铜离子,还含有能够与铁反应的离子,结合选项可知应该为铁离子;根据反应Fe+2Fe3+=3Fe2+可知,0.05mol铁粉会消耗0.1mol铁离子,所以混合物中铜离子与铁离子的物质的量之比为1:1;该浓酸应该为浓硝酸,生成的气体为二氧化碳和二氧化氮气体,据此对各选项进行判断.
解答 解:6.4g红色沉淀为Cu,其物质的量为:$\frac{6.4g}{64g/mol}$=0.1mol,根据反应Fe+Cu2+=Fe2++Cu可知,生成0.1mol铜需要消耗0.1mol还原铁粉,而实际上消耗了0.15mol铁粉,则反应后的溶液中除了含有铜离子,还含有能够与铁反应的离子,结合选项可知应该为铁离子;根据反应Fe+2Fe3+=3Fe2+可知,0.05mol铁粉会消耗0.1mol铁离子,所以混合物中铜离子与铁离子的物质的量之比为1:1;
将上述生成的两种气体通入足量饱和NaHCO3溶液中,仍然收集到两种气体,该浓酸应该为浓硝酸,生成的气体为二氧化碳和二氧化氮气体,
根据分析可知,满足条件的只有B,
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应原理为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力,

练习册系列答案
相关题目
17.雷美替胺是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法正确的是( )
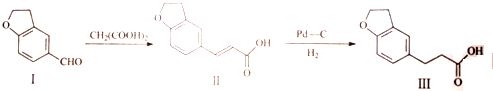

| A. | 可用浓溴水区分化合物Ⅱ和化合物Ⅲ | |
| B. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| C. | 1mol化合物Ⅰ最多能与3molH2发生加成反应 | |
| D. | 与化合物Ⅰ互为同分异构体,且分子含有2个醛基的芳香族化合物有10种 |
18.现有X、Y、Z、M四种短周期元素,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍.下列说法不正确的是( )
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的稳定性:Z<M | |
| C. | 简单离子半径由大到小的顺序是:Z>M>Y | |
| D. | 等浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z<Y2Z |
15.短周期元素X、T、Y、Z、R原子序数依次增大,T最内层电子数为最外层的2倍,部分元素的化合价关系如下表.则下列判断正确的是( )
| X | Y | Z | R | |
| 主要化合价 | -4,+4 | -4,+4 | -2,+6 | -1,+7 |
| A. | 非金属性:Z<R<Y | |
| B. | T与R可以形成化合物:TR2 | |
| C. | X与R的单质均能使品红溶液褪色,且褪色原理相同 | |
| D. | T的最高价氧化物的水化物分别能与X、Y、Z的最高价氧化物反应 |
2.下列有关说法正确的是( )
| A. | 已知I2可溶于KI形成KI3,向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀,说明KI3溶液中存在平衡:I3-?I2+I- | |
| B. | 物质的量浓度相等的H2CO3和Na2CO3溶液等体积混合后的溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| C. | 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2.0×10-12,将等体积的浓度为1.0×10-4mol/L的AgNO3溶液滴入到浓度均为1.0×10-4mol/L的KCl和K2CrO4的混合溶液中产生两种不同沉淀,且Ag2CrO4沉淀先产生 | |
| D. | 25℃时,溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14 |
12.将足量的气体通入下列各溶液中,所含离子或分子还能大量共存的是( )
| A. | 通入足量SO2:Na+、S2-、OH-、AlO2- | B. | 通入足量CO2:K+、Ca2+、Cl-、NO3- | ||
| C. | 通入足量Cl2:SO2、Ba2+、Cl-、K+ | D. | 通入足量NH3:Fe3+、Cl-、Ba2+、Al3+ |
19.如图为实验室中完成不同化学实验的示意图,其中正确的是( )

| A. | 图①常用于分离沸点相差较大的液体混合物 | |
| B. | 图②用于吸收尾气SO2 | |
| C. | 图③用于干燥、收集少量NH3 | |
| D. | 采用图④的操作排出碱式滴定管尖嘴处的气泡 |
3.已知可逆反应温度为T0时,在容积固定的密闭容器中发生 X(g)+Y(g)?Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a 所示.其他条件相同,温度分别为 T1、T2时发生反应;Z 的浓度随时间变化的关系如图b 所示.下列叙述正确的是( )
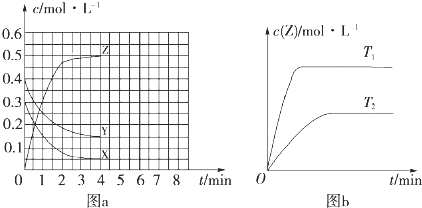

| A. | 发生反应时,各物质的反应速率大小关系为v(X)=v (Y)=2 v (Z) | |
| B. | 图a 中反应达到平衡时,Y 的转化率为37.5% | |
| C. | T0 时,该反应的平衡常数为 33.3 | |
| D. | 该反应正反应的反应热△H<0 |