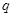题目内容
用化学反应原理相关知识同答
I.根据下表所示化学反应与数据关系回答下列问题:
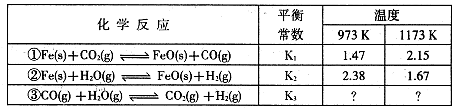
(1)反应①是 (填“吸热"或“放热”)反应。
(2)根据反应①与②可推导出同温下K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
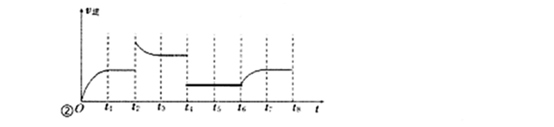
(3)若反应③的逆反应速率与时间的关系如图所示:
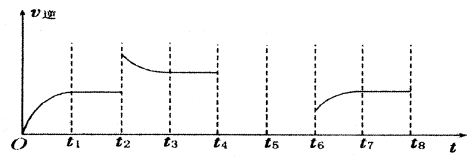
①反应在t1、t3、t7时都达到了平衡,若t2时只改变了一种外界条件j试判断:改变的条件可能是 。
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。
II.请根据醋酸的电离平衡回答下列问题:
(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH= 。
(2)将上述溶液加蒸馏水稀释,在稀释过程中,下列各项中增大的是 (填字母编号)。
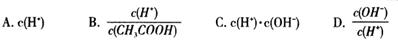
(3)25℃时,CH3COOH的电离平衡常数为1.75×10-5,现将一定量的CH3COOH与NaOH溶液混合,若测得混合液pH=5.6,则混合液中各离子浓度由大到小的顺序是 。
I.根据下表所示化学反应与数据关系回答下列问题:

(1)反应①是 (填“吸热"或“放热”)反应。
(2)根据反应①与②可推导出同温下K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
(3)若反应③的逆反应速率与时间的关系如图所示:

①反应在t1、t3、t7时都达到了平衡,若t2时只改变了一种外界条件j试判断:改变的条件可能是 。
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。
II.请根据醋酸的电离平衡回答下列问题:
(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH= 。
(2)将上述溶液加蒸馏水稀释,在稀释过程中,下列各项中增大的是 (填字母编号)。
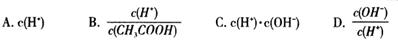
(3)25℃时,CH3COOH的电离平衡常数为1.75×10-5,现将一定量的CH3COOH与NaOH溶液混合,若测得混合液pH=5.6,则混合液中各离子浓度由大到小的顺序是 。
Ⅰ
(1)吸热
K2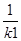
①升高温度或增大CO2的浓度(增大H2的浓度)
②
Ⅱ、(1)3
(2)BD
(3) c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
(1)吸热
K2
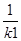
①升高温度或增大CO2的浓度(增大H2的浓度)
②

Ⅱ、(1)3
(2)BD
(3) c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
试题分析:Ⅰ(1)升高温度,平衡常数增大,正反应是吸热反应。
K3=
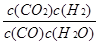 而K1=
而K1=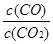 ,K2=
,K2= 故K3=K2X
故K3=K2X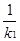
(3)?升高温度或增大CO2的浓度(增大H2的浓度)
Ⅱ、(1)根据c(H+)=c(HAc)ɑ,则c(H+)=0.1X1%,PH=3
电离常数不变,c(H+)在稀释过程中总体是减小的;水的离子积常数不变;c(H+)减小,则c(OH-)增大,故选BD。
(3)据题意,混合溶液的PH为5.6,溶液显弱酸性,则有 c(CH3COO-)>c(Na+)>c(H+)>c(OH-)

练习册系列答案
相关题目
 2NO2(g),经5min达到平衡,测得c(NO)=0.5mol/L,并放热Q kJ。
2NO2(g),经5min达到平衡,测得c(NO)=0.5mol/L,并放热Q kJ。 v
v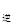 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 ,可以在强碱性条件下加入铝粉除去(反应过程中无气态产物生成。加热反应后的溶液有能使湿润的红色石蕊试纸变蓝的气体逸出)。请写出该反应的离子方程式____ 。
,可以在强碱性条件下加入铝粉除去(反应过程中无气态产物生成。加热反应后的溶液有能使湿润的红色石蕊试纸变蓝的气体逸出)。请写出该反应的离子方程式____ 。 M(g)+N(s) ΔH<0,达到平衡时,下列说法正确的是
M(g)+N(s) ΔH<0,达到平衡时,下列说法正确的是 2SO3达平衡后,改变某一条件K值不变,SO2的转化率可能增大、减小或不变
2SO3达平衡后,改变某一条件K值不变,SO2的转化率可能增大、减小或不变 H++Cl-+HClO。下列说法中确的是
H++Cl-+HClO。下列说法中确的是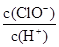 增大
增大
 2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小
2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小 HCO3-+OH一,升高温度溶液碱性增强
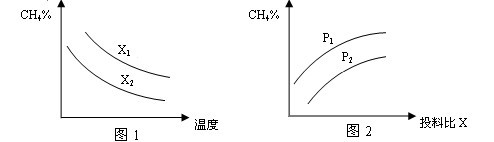
HCO3-+OH一,升高温度溶液碱性增强 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是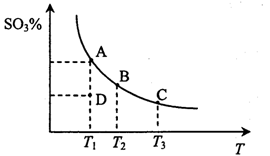
 pC(g) △H,结合图中所给的信息填空。
pC(g) △H,结合图中所给的信息填空。
 ______
______
 ______
______
 ______
______