题目内容
14.某化学课外活动小组用硫酸铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,进行如下实验.制备硫酸亚铁晶体主要的操作流程如下:
请根据题目要求回答下列问题:
(1)A的化学式为Fe.上述操作过程中用到的玻璃仪器有:
①烧杯;②玻璃棒;③酒精灯;④温度计;⑤漏斗.
(2)趁热过滤的目的是防止硫酸亚铁晶体析出.
(3)结晶操作过程中应控制滤液酸性的原因是抑制Fe2+离子水解.
(4)已知硫酸亚铁铵[(NH4)2Fe(SO4)2]比硫酸亚铁稳定,常用在分析化学中.硫酸亚铁铵可用硫酸亚铁和硫酸铵反应制得.实验室利用硫酸亚铁铵溶液和草酸溶液反应生成草酸亚铁沉淀来制备草酸亚铁.写出硫酸亚铁铵溶液和草酸溶液反应的离子方程式:Fe2++H2C2O4=FeC2O4↓+2H+.
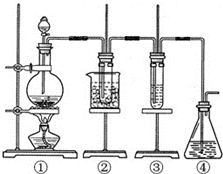
(5)草酸亚铁晶体(相对分子质量:180)受热易分解.某课外活动小组设计如图的实验装置来检验其分解产物.

①该设备中最不合理的部分是(填字母)A,原因是反应生成的水易沿试管壁流下使试管炸裂.
②改用正确装置,实验开始后,B处变蓝色,说明草酸亚铁晶体中有结晶水;C处有白色沉淀,E处部分黑色粉末变为红色,说明草酸亚铁分解产生(填化学式,下同)CO、CO2;反应后在A处试管中有黑色固体粉末(混合物)产生,倒出时有燃烧现象.A处试管中的黑色固体粉末可能是Fe、FeO.
分析 (1)加入过量的铁粉,与Fe3+、Cu2+、H+离子反应转化为Fe2+;过滤使用的主要玻璃仪器是普通漏斗;
(2)趁热过滤的目的是:要避免某些成分在过滤过程中因遇冷而结晶或沉淀;
(3)应从盐类水解的角度考虑,防止硫酸亚铁水解造成损耗;
(4)由题意可知(NH4)2Fe(SO4)2与草酸反应的方程式:(NH4)2Fe(SO4)2+H2C2O4=FeC2O4↓+(NH4)2SO4+H2SO4;
(5)根据草酸亚铁晶体的相对分子质量为180,得其化学式为FeC2O4•2H2O,加热时有水产生,故A装置最不合理,因为大试管管口略向上倾斜,产生的水会回流使试管炸裂,根据B、C、E判断产物有H2O(或结晶水)、CO2、CO,其中CO的存在使高价铁不可能存在,考虑“黑色固体混合物粉末”,应是Fe与FeO的混合,燃烧现象应是温度较高时Fe的燃烧情况.
解答 解:(1)加入过量的铁粉,与Fe3+、Cu2+、H+离子反应转化为Fe2+;过滤使用的主要玻璃仪器有:烧杯、玻璃棒、普通漏斗,
故答案为:Fe;漏斗;
(2)趁热过滤的目的是:要避免某些成分在过滤过程中因遇冷而结晶或沉淀,
故答案为:防止硫酸亚铁晶体析出;
(3)亚铁离子可以水解,结晶操作过程中控制滤液的酸性,可以抑制硫酸亚铁水解造成损耗,
故法案为:抑制Fe2+离子水解;
(4)由题意可知(NH4)2Fe(SO4)2与草酸反应的方程式:(NH4)2Fe(SO4)2+H2C2O4=FeC2O4↓+(NH4)2SO4+H2SO4,故反应离子方程式为:Fe2++H2C2O4=FeC2O4↓+2H+,
故答案为:Fe2++H2C2O4=FeC2O4↓+2H+;
(5)根据草酸亚铁晶体的相对分子质量为180,得其化学式为FeC2O4•2H2O.
①加热时有水产生,故A装置最不合理,因为大试管管口略向上倾斜,产生的水会回流使试管炸裂,
故答案为:A;反应生成的水易沿试管壁流下使试管炸裂;
②改用正确装置,实验开始后,B处变蓝色,说明草酸亚铁晶体中有结晶水;C处有白色沉淀,E处部分黑色粉末变为红色,说明草酸亚铁分解产生:CO、CO2;CO的存在使高价铁不可能存在,考虑“黑色固体混合物粉末”,应是Fe与FeO的混合,燃烧现象应是温度较高时Fe的燃烧情况,
故答案为:结晶水;CO、CO2;Fe、FeO.
点评 本题以硫酸亚铁晶体的制备为载体,主要考查了除杂提纯的基本操作、对实验步骤原理和目的分析评价、对装置的分析评价等,明确原理是解题关键,弄清所发生的化学反应及铁元素存在形态的变化.

| A. | 对于2SO2(g)+O2(g)?2SO3(g)△H=QKJ/mol(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ | |
| B. | 热化学方程式中的化学计量数表示相应物质的物质的量,不能用分数表示 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 小苏打在水中的电离方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ |
 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(结构简式如图)是这种饮料的主要酸性物质.下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(结构简式如图)是这种饮料的主要酸性物质.下列相关说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 1mol苹果酸和足量的钠反应生成1.5moL的H2 | |
| D. | 1mol苹果酸与Na2CO3溶液反应必需消耗2mol Na2CO3 |
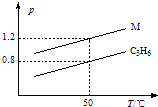 图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试据图形判断M气体可能是( )
图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试据图形判断M气体可能是( )| A. | SO2 | B. | CO2 | C. | C3H8 | D. | CO和N2 |
| A. | 2一甲基丁烷 | B. | 2一甲基丙烷 | C. | 2,2一二甲基丙烷 | D. | 2一乙基丙烷 |
 乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.
乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.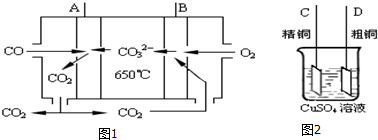
 ;
; ;
; .
. 某学习小组设计了如图所示的实验方案来制取次氯酸钠和探究氯水的性质.图中:
某学习小组设计了如图所示的实验方案来制取次氯酸钠和探究氯水的性质.图中: