题目内容
【题目】下列含有共价键的离子化合物是( )
A. HIB. NaOHC. Br2D. NaCl
【答案】B
【解析】
A.HI是共价化合物,故A错误;
B. NaOH是由Na+和OH-通过离子键形成的离子化合物,OH-内存在O-H共价键,故B正确;
C. Br2是含有共价键的单质,故C错误;
D. NaCl是由Na+和Cl-通过离子键形成的离子化合物,没有共价键,故D错误;
答案:B

练习册系列答案
相关题目
【题目】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka=1.75×10﹣5 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1= .
(2)在相同条件下,试比较H2CO3、HCO3﹣和HSO3﹣的酸性强弱:>>
(3)①如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是(填化学式).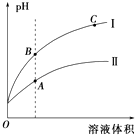
②a、b、c三点中,水的电离程度最大的是(填字母).