题目内容
2.下列反应中,氧化剂与还原剂物质的量之比为1:2的是( )| A. | 3S+6NaOH═2Na2S+Na2SO3+3H2O | |
| B. | 2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)2 | |
| C. | I2+2NaClO3═2NaIO3+Cl2 | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O |
分析 含有元素化合价降低的物质为氧化剂,含有元素化合价升高的物质为还原剂,结合反应方程式中元素化合价的变化分析.
解答 解:A.3S+6NaOH═2Na2S+Na2SO3+3H2O反应中有2molS化合价降低,作氧化剂,有1molS升高作还原剂,则氧化剂与还原剂物质的量之比为2:1,故A错误;
B.2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)2反应中没有元素化合价的变化,不是氧化还原反应,故B错误;
C.I2+2NaClO3═2NaIO3+Cl2反应中,NaClO3作氧化剂,I2作还原剂,则氧化剂与还原剂物质的量之比为2:1,故C错误;
D.4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O反应中,当1molMnO2得到2mol电子时,有2molHCl失电子,则氧化剂与还原剂物质的量之比为1:2,故D正确.
故选D.
点评 本题考查氧化还原反应概念及计算,判断氧化剂、还原剂后,可以根据电子转移守恒计算氧化剂和还原剂的物质的量之比,难度不大.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 | |
| B. | 根据原子核外电子排布的特点,Cu属于s区元素 | |
| C. | 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 | |
| D. | 核外电子排布由1s22s22p63s1-→1s22s22p6 的变化需要吸收能量 |
13.下列关于有机实验说法正确的是( )
| A. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行两次过滤操作 | |
| B. | 实验室制乙烯时,为减弱浓硫酸对有机物的碳化作用,应用小火缓慢加热 | |
| C. | 在石油的分馏、制硝基苯、制乙烯的实验中,都要使温度计的水银液泡浸入反应液中,以控制实验温度 | |
| D. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 |
10.等质量的下列物质分别与足量的盐酸反应,放出二氧化碳气体最多的是( )
| A. | Ca(HCO3)2 | B. | NaHCO3 | C. | Na2CO3 | D. | CaCO3 |
17.下列化学用语表示正确的是( )
| A. | 铝原子的结构示意图: | B. | 乙炔的比例模型: | ||
| C. | 水分子的电子式: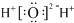 | D. | 硝基苯的结构简式: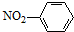 |
7.把有机物的混合物在一定条件下反应:
①1,3一丁二烯与溴水的加成产物,
②乙二醇与乙酸酯化得酯,
③甘氨酸与丙氨酸生成二肽,
④苯酚和浓溴水.反应所生成的有机物的种类由多到少的顺序是( )
①1,3一丁二烯与溴水的加成产物,
②乙二醇与乙酸酯化得酯,
③甘氨酸与丙氨酸生成二肽,
④苯酚和浓溴水.反应所生成的有机物的种类由多到少的顺序是( )
| A. | ④③②① | B. | ①②③④ | C. | ③①②④ | D. | ③②①④ |
14.一定能在下列溶液中大量共存的离子组是( )
| A. | 澄清溶液:Fe3+、NH4+、Cl-、ClO- | |
| B. | pH=1的溶液:Na+、Mg2+、Ca2+、NO3- | |
| C. | 滴加酚酞显红色的溶液:K+、Cl-、Br-、HCO3- | |
| D. | 亚硫酸钠溶液:K+、SO42-、NO3-、H+ |
12.下列各组离子在溶液中能大量共存的是( )
| A. | Ba2+、C1-、CO32-、K+ | B. | K+、OH-、HCO${\;}_{3}^{-}$、Na+ | ||
| C. | H+、Fe2+、MnO4-、Cl- | D. | Ca2+、HCO${\;}_{3}^{-}$、C1-、K+ |