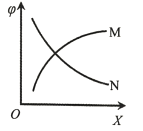
��Ŀ����
����Ŀ���л���F������ij����Ѫҩ���Ʊ�����ҵ����F��һ��·��ͼ���£�����H��FeCl3��Һ�ܷ�����ɫ��Ӧ����
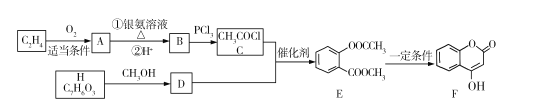
�ش��������⣺
(1)A�������� ___��E�еĹ�������������____��
(2)B��C�ķ�Ӧ������ ___��F�ķ���ʽΪ____��
(3)H�Ľṹ��ʽΪ ___��
(4)E��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ___��
(5)ͬʱ��������������D��ͬ���칹�干��____�֣�д���˴Ź���������5�������ʵĽṹ��ʽ ___
���Ƿ����廯����
������NaHCO3��Һ��Ӧ
������FeCl3��Һ����ɫ
��1mol���������Ʒ�Ӧʱ���ɵõ�1molH2
(6)��2�ȱ��ᡢ����Ϊԭ���Ʊ��۱�ϩ�ᱽ����(![]() )��д���ϳ�·��ͼ�����Լ���ѡ��_________��
)��д���ϳ�·��ͼ�����Լ���ѡ��_________��
���𰸡���ȩ ������ ȡ����Ӧ C9H6O3 ![]()
 4
4 ![]()

��������
��A������֪������ȩ����ȩ������Ϊ���ᣬ������PCl3����ȡ����Ӧ����C����H��D��E��ת����ϵ��E��C�Ľṹ��ʽ����֪HΪ![]() ��DΪ
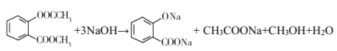
��DΪ![]() ��E�����к���2����������NaOH��Һ��Ӧ����
��E�����к���2����������NaOH��Һ��Ӧ����![]() ��CH3COONa��CH3OH��H2O���ɢ�֪�����к��б������ɢ�֪�����к���-COOH�Ҳ������ǻ����ɢ�֪�����л����д��ǻ�����������ֻ��һ��ȡ����ʱ��ȡ����Ϊ-CHOHCOOH����������������ȡ����ʱ������ȡ�����ֱ�Ϊ-CH2OH��-COOH������ȡ�����ڱ�����3��λ�ù�ϵ���ʹ���4��ͬ���칹�塣���к˴Ź���������5����������
��CH3COONa��CH3OH��H2O���ɢ�֪�����к��б������ɢ�֪�����к���-COOH�Ҳ������ǻ����ɢ�֪�����л����д��ǻ�����������ֻ��һ��ȡ����ʱ��ȡ����Ϊ-CHOHCOOH����������������ȡ����ʱ������ȡ�����ֱ�Ϊ-CH2OH��-COOH������ȡ�����ڱ�����3��λ�ù�ϵ���ʹ���4��ͬ���칹�塣���к˴Ź���������5����������![]() ��2-�ȱ����ȷ�����ȥ��Ӧ�õ���ϩ���ƣ��ữ����PCl3��Ӧ�õ�CH2=CHCOCl�����뱽�ӷ���ȡ����Ӧ��������Ӿ۷�Ӧ���ɡ��ݴ˷�����
��2-�ȱ����ȷ�����ȥ��Ӧ�õ���ϩ���ƣ��ữ����PCl3��Ӧ�õ�CH2=CHCOCl�����뱽�ӷ���ȡ����Ӧ��������Ӿ۷�Ӧ���ɡ��ݴ˷�����
(1)��ϩ������������A��A�ܹ���������Һ��Ӧ���ɴ˿�֪AΪ��ȩ����E�Ľṹ��ʽ��֪E�еĹ�����Ϊ��������Ϊ����ȩ��������
(2)��ȩ������������Һ��Ӧ���������ƣ��پ����ữ�������ᣬ��BΪ���ᣬ������PCl3������Ӧ����C����C�Ľṹ��֪�������е�-OH��Clԭ��ȡ������C����Ӧ����Ϊȡ����Ӧ����F�Ľṹ��ʽ��֪��F�ķ���ʽΪ��C9H6O3����Ϊ��ȡ����Ӧ��C9H6O3��
(3)��H��D��E��ת����ϵ��E��C�Ľṹ��ʽ����֪HΪ![]() ����Ϊ��
������![]() ��
��
(4)E�к���2����������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ�� ����Ϊ��
������ ��
��
(5)��E�Ľṹ��H�Ľṹ��֪��D�Ľṹ��ʽΪ![]() ���ɢٿ�֪�����к��б������ɢڿ�֪�����к���-COOH�Ҳ������ǻ����ɢۿ�֪�����л����д��ǻ�(����л������ܲ����Ͷ�Ϊ5������ռ4�������Ͷȣ��Ȼ�ռ1�������Ͷȣ���һ���ܹ����Ʒ�Ӧ����H2�Ĺ�����Ϊ�ǻ�)��������������л���Ϊ��
���ɢٿ�֪�����к��б������ɢڿ�֪�����к���-COOH�Ҳ������ǻ����ɢۿ�֪�����л����д��ǻ�(����л������ܲ����Ͷ�Ϊ5������ռ4�������Ͷȣ��Ȼ�ռ1�������Ͷȣ���һ���ܹ����Ʒ�Ӧ����H2�Ĺ�����Ϊ�ǻ�)��������������л���Ϊ��![]() ��1�֣���
��1�֣���![]() ���ڼ�Թ�3�֣����ʹ���4�ֽṹ�����к˴Ź���������5��壬����ͬ��ѧ��������ԭ����5�֣�������Ϊ��
���ڼ�Թ�3�֣����ʹ���4�ֽṹ�����к˴Ź���������5��壬����ͬ��ѧ��������ԭ����5�֣�������Ϊ��![]() ���ʴ�Ϊ��4��
���ʴ�Ϊ��4��![]() ��
��
(6)![]() �ĵ���Ϊ��
�ĵ���Ϊ��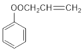 ����CH3CHClCOOH�ͱ���Ϊԭ�ϣ����Ⱥϳ�
����CH3CHClCOOH�ͱ���Ϊԭ�ϣ����Ⱥϳ�![]() ��Ȼ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�ᱽ��������ϳ�·��ͼΪ��
��Ȼ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�ᱽ��������ϳ�·��ͼΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ��

����Ŀ��̼��������Ҫ�ķǽ���Ԫ�أ����������������й㷺��Ӧ�á�
(1)��ֲ֪�������÷����ķ�Ӧ���£�6CO2(g)��6H2O(l) ![]() C6H12O6(s)��6O2(g) ��H����669.62 kJmol��1�÷�Ӧ�ﵽ��ѧƽ������ı�����������CO2ת�����������__________��
C6H12O6(s)��6O2(g) ��H����669.62 kJmol��1�÷�Ӧ�ﵽ��ѧƽ������ı�����������CO2ת�����������__________��
a������CO2��Ũ�� b��ȡ��һ��C6H12O6
c��������� d���ʵ������¶�
(2)N2O5�ķֽⷴӦ2N2O5(g)![]() 4NO2(g) + O2(g)����ʵ������67��ʱN2O5��Ũ����ʱ��ı仯���£�
4NO2(g) + O2(g)����ʵ������67��ʱN2O5��Ũ����ʱ��ı仯���£�
ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 |
c(N2O5) /(molL��1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
������0��2minʱ�Σ���ѧ��Ӧ����v(NO2) ��________molL-1min-1��
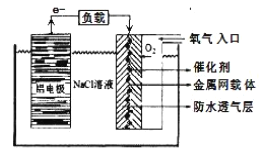
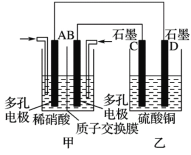
(3)����NO2��O2ͨ�������Ƴ���ͼ��ʾװ�ã�D�缫���к�ɫ������������A�缫��ͨ�������Ϊ_________���ѧʽ����A�缫�ĵ缫��ӦʽΪ_______________________��һ��ʱ������������0.2 mol Cu(OH)2ʹ��Һ��ԭ����ת�Ƶĵ��ӵ����ʵ���Ϊ _____________��
(4)����CO��NO����ͬ����Ͷ��һ�ܱ������з�����Ӧ��2CO(g)��2NO(g)![]() N2(g)��2CO2(g)����H����759.8 kJ��mol��1����Ӧ�ﵽƽ��ʱ��N2�����������n(CO)/n(NO)�ı仯��������ͼ
N2(g)��2CO2(g)����H����759.8 kJ��mol��1����Ӧ�ﵽƽ��ʱ��N2�����������n(CO)/n(NO)�ı仯��������ͼ
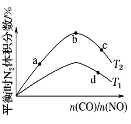
��b��ʱ��ƽ����ϵ��C��Nԭ�Ӹ���֮�Ƚӽ�________________��
��a��b��c����CO��ת���ʴӴ�С��˳��Ϊ____________��a��c��d�����ƽ�ⳣ���Ӵ�С��˳��Ϊ__________________��
����![]() ��0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����CO��ת����Ϊ___________��
��0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����CO��ת����Ϊ___________��