题目内容
【题目】甲硅烷广泛用于电子工业、汽车领域,三氯氢硅(SiHCl3)是制备甲硅烷的重要原料。回答下列问题:
(1)工业上以硅粉和氯化氢气体为原料生产SiHCl3时伴随发生的反应有:
Si(s)+4HCl(g)=SiCl4(g)+2H2(g) H=-241kJ/mol
SiHCl3(g)+HCl(g)=SiCl4(g)+H2(g) H=-31kJ/mol
以硅粉和氯化氢气体生产SiHCl3的热化学方程式是 ___。
(2)铝锂形成化合物LiAlH4既是金属储氢材料又是有机合成中的常用试剂,遇水能得到无色溶液并剧烈分解释放出H2,请写出其水解反应化学方程式____。LiAlH4在化学反应中通常作_______(填“氧化”或“还原”)剂。工业上可用四氯化硅和氢化铝锂(LiAlH4)制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为 _________
(3)三氯氢硅歧化也可制得甲硅烷。反应2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PA100催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。
SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PA100催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。
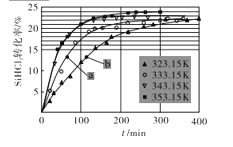
①353.15K时,平衡转化率为____,该反应是____反应(填“放热”“吸热”)。
②323.15K时,要缩短反应达到平衡的时间,可采取的最佳措施是____。
(4)比较a、b处反应速率的大小:Va ___Vb (填“>”“<”或“=”)。已知反应速率V正=K1x2SiHCl3,V逆=K2xSiH2Cl2xSiCl4,K1,K2分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在353.15K时K1/K2 =____(保留3位小数)。
(5)硅元素最高价氧化物对应的水化物是H2SiO3,室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是 ___,其原因是____。已知:H2SiO3 :Ka1=2.0×10-10、Ka2=2.0×10-12、H2CO3 :Ka1=4.3×10-7,Ka2=5.6×10-11
【答案】Si(s)+3HCl(g)= SiHCl3(g)+H2(g) H=-210kJ/mol LiAlH4+2H2O=4H2↑+LiAlO2 还原 LiAlH4+ SiCl4= SiH4+ LiCl+AlCl3 24% 吸热 改进催化剂 > 0.025 硅酸钠 硅酸的Ka2小于碳酸的Ka2,硅酸钠更易水解
【解析】
根据盖斯定律书写热化学方程式;水解方程式是LiAlH4与水反应生成氢气和偏铝酸锂,LiAlH4与四氯化硅反应生成两种盐,根据金属元素可推出为LiCl、AlCl3;由图可知353.15K时,平衡转化率最大为24%,同时可得温度升高,平衡转化率增大,说明平衡正向移动;a、b两处转化率相同,时间不同,根据时间长短可判断速率快慢;根据平衡时正逆反应速率相等,可求出K值与K1、K2的关系,进而计算出K1与K2的比值;根据越弱越水解原则判断溶液的碱性强弱;据此分析。
(1)Si(s)+4HCl(g)=SiCl4(g)+2H2(g) H=-241kJ/mol ①;SiHCl3(g)+HCl(g)=SiCl4(g)+H2(g) H=-31kJ/mol ②;根据盖斯定律,①-②得硅粉和氯化氢气体生产SiHCl3的热化学方程式:Si(s)+3HCl(g)= SiHCl3(g)+H2(g) H=-210kJ/mol;答案为:Si(s)+3HCl(g)= SiHCl3(g)+H2(g) H=-210kJ/mol;
(2) LiAlH4遇水能得到无色溶液并剧烈分解释放出H2,则水解反应化学方程式为:LiAlH4+2H2O=4H2↑+LiAlO2;LiAlH4中H是-1价,在化学反应中常作还原剂;四氯化硅和LiAlH4反应后得甲硅烷及两种盐,LiAlH4中有2种金属元素,所以生成的2种盐为氯化铝和氯化锂,化学方程式为:LiAlH4+ SiCl4= SiH4+ LiCl+AlCl3;答案为:LiAlH4+2H2O=4H2↑+LiAlO2;还原;LiAlH4+ SiCl4= SiH4+ LiCl+AlCl3;
(3)①根据图得353.15K时,平衡转化率最大为24%,则转化率为24%;同时可得温度升高,平衡转化率增大,说明平衡正向移动,正向为吸热反应;答案为:24%;吸热;
②323.15K时,要缩短反应达到平衡的时间即加快反应速率,可采取的最佳措施是改进催化剂;答案为:改进催化剂;
(4)a、b两处转化率相同,说明消耗的SiHCl3等量,时间不同,时间越短速率越快,则Va>Vb;已知反应速率V正=K1x2SiHCl3,V逆=K2xSiH2Cl2xSiCl4,达到平衡时V正= V逆,即K1x2SiHCl3= K2xSiH2Cl2xSiCl4,变式得![]() ==
==![]() =K,由图可得平衡时转化率为24%,三段式表示为:
=K,由图可得平衡时转化率为24%,三段式表示为: ,
,![]() ,则在353.15K时
,则在353.15K时![]() =0.025;答案为:>;0.025;
=0.025;答案为:>;0.025;
(5)根据硅酸和碳酸的2级电离常数可得,H2SiO3的Ka2=2.0×10-12,小于H2CO3的Ka2=5.6×10-11,越弱越水解原则得硅酸根离子水解程度大于碳酸根离子水解程度,所以室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是硅酸钠;答案是:硅酸钠;硅酸的Ka2小于碳酸的Ka2,硅酸钠更易水解。