题目内容
【题目】氯酸钾是常见的氧化剂,用于制造火药、烟火。工业上用石灰乳氯化法制备氯酸钾的流程如图所示:
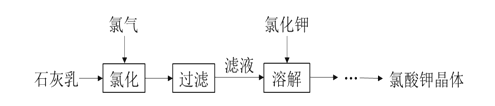
已知:氯化过程主要发生反应:![]()
完成下列填空:
(1)工业生产氯气的方法是________(请用文字表述)。
(2)氯化过程需要控制较高温度,其目的有:①_______;②减少Cl2与Ca(OH)2之间的副反应。
(3)向热的滤液中加入稍过量的氯化钾,待溶解完全后进行冷却,有大量氯酸钾晶体析出,写出相关反应的化学方程式:______。得到的氯酸钾晶体中可能会含有少量氯化钾,进一步提纯的方法是_______。
(4)为测定所得晶体中氯酸钾的纯度,将a g样品与b g二氧化锰混合,加热该混合物一段时间后(杂质不参加反应)冷却,称量剩余固体质量,重复加热、冷却、称量操作,记录数据如下表:
加热次数 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | c | d | e | e |
(i)进行加热操作时,应将固体置于________(填仪器名称)中。
(ii)该实验不必进行第五次加热的原因是_______。
(iii)若某次测定结果的相对误差为-2.98%,写出导致这一结果的一种可能情况。______。
【答案】电解饱和食盐水 加快反应速率 Ca(ClO3)2 +2KCl=CaCl2+2KClO3↓ 重结晶 坩埚 剩余固体质量已恒重,说明KClO3已分解完全 ①未在干燥器中冷却,剩余固体吸水②加热时间不足,氯酸钾未完全分解(任写一种)
【解析】
(1)工业用电解饱和食盐水的方法生产氯气;
(2)温度升高有利于加快反应速率;
(3)热的氯酸钙与氯化钾反应生成溶解度更小的氯酸钾,用重结晶的方法可提纯氯酸钾晶体;
(4)(i)灼烧固体在坩埚中进行;
(ii)第三次和第四次的固体质量恒重,说明分解完全;
(iii)若某次测定结果的相对误差为-2.98%,说明所得数据偏小,可能为剩余固体质量偏大,据此分析。
(1)在工业上一般用电解饱和食盐水的方法生产氯气,反应方程式为: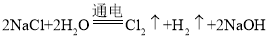 ;
;
(2)为加快反应速率,减少 Cl2与 Ca(OH)2之间发生副反应生成次氯酸钙,氯化过程需在较高的温度下进行;
(3)热的氯酸钙与氯化钾发生复分解反应生成溶解度更小的氯酸钾,反应为:Ca(ClO3)2 +2KCl=CaCl2+2KClO3↓;若反应得到的氯酸钾晶体中含有少量氯化钾,进一步提纯的方法可根据氯酸钾的溶解度受温度的影响变化较大,用重结晶的方法纯氯酸钾晶体;
(4)(i)灼烧固体要在坩埚中进行;
(ii)由表中数据可知,第三次和第四次的剩余固体质量已恒重,说明 此时KClO3已分解完全,因此无需再做第五次加热操作;
(iii)若某次测定结果的相对误差为-2.98%,说明所得数据偏小,可能为剩余固体质量偏大,可能为未在干燥器中冷却,剩余固体吸水(加热时间不足,氯酸钾未完全分解)。

 阅读快车系列答案
阅读快车系列答案【题目】根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。非特殊说明,书写离子方程式)
实验现象 | 离子方程式 |
1.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 | ______ |
2.制备氢氧化铁胶体的化学方程式 | ______ |
3.二氧化硫使酸性高锰酸钾溶液褪色 | ______ |
4.Fe3O4溶于稀硝酸 | ______ |
5.氯化亚铁溶液通入少量氯气,变为黄色溶液,加入过量碘化钾溶液,溶液颜色加深,继续加入NaOH溶液,出现白色沉淀,且颜色不断加深至红褐色。 | ______ |
6.澄清石灰水中通入CO2出现白色沉淀,继续通入二氧化碳,沉淀溶解,加热后又出现白色沉淀。 | ______ |
7.三氯化铝溶液中加逐滴加入NaOH溶液,先出现白色沉淀,然后溶解,再通入CO2至刚开始出现沉淀。 | ______ |
8.NH4Al(SO4)2溶液与Ba(OH)2溶液物质的量1∶2混合 | ______ |
9.FeI2与Cl2物质的量1∶2反应 | ______ |
10.Ba(OH)2中加入硫酸铝溶液,至沉淀质量不再改变。再加入过量NaHCO3溶液,又出白色沉淀。 | ______ |
11.生产硫化钠大多采用无水芒硝(Na2SO4)—碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式 | ______ |
12.温度高于200 ℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4∶1),写出该反应的化学方程式 | ______ |
13.湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 | ______ |