题目内容
17.草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液.称25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol•L-1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O,试回答:(1)实验中不需要的仪器有(填序号)cf,还缺少的仪器有(填名称)铁架台(带滴定管夹).
a.托盘天平(带砝码,镊子) b.滴定管 c.100mL量筒 d.100mL容量瓶 e.烧杯 f.漏斗 g.锥形瓶 h.玻璃棒球 i.药匙 j.烧瓶
(2)实验中,标准液KMnO4溶液应装在酸式滴定管中,因为KMnO4溶液有强氧化性,能腐蚀碱式滴定管中的橡皮管.
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会无影响(偏大、偏小、无影响)
(4)在滴定过程中若用amol•L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为0.1aVmol•L-1,由此可计算x的值是$\frac{50W}{9aV}$-5.
分析 (1)实验有两个过程:配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;
用高锰酸钾溶液进行滴定测草酸的物质的量:所需要的实验仪器主要有烧杯、酸式滴定管、铁架台(带滴定管夹)、锥形瓶等;根据以上操作中使用的仪器进行解答;
(2)KMnO4溶液具有强氧化性,能够腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
(3)根据实验操作对c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$的影响分析误差;
(4)根据化学方程式中各物质的关系进行计算出草酸的浓度,从而计算出样品中含有草酸的质量、结晶水的质量,最后计算出草酸晶体中x值.
解答 解:(1)为了准确配制一定浓度浓度的草酸溶液,所需要的实验仪器主要为:天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;
用高锰酸钾溶液进行滴定测草酸的物质的量,所需要的实验仪器主要有:烧杯、酸式滴定管、铁架台(带滴定管夹)、锥形瓶等,
则在以上操作中不需要的仪器有:c.100mL量筒、f.漏斗;还缺少的仪器为:铁架台(带滴定管夹),
故答案为:cf;铁架台(带滴定管夹);
(2)KMnO4溶液具有强氧化性,可以腐蚀碱式滴定管中的橡皮管,故KMnO4溶液应装在酸式滴定管中,
故答案为:酸;KMnO4溶液有强氧化性,能腐蚀碱式滴定管中的橡皮管;
(3)在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,蒸馏水不影待测液的物质的量,对V(标准)无影响,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知,c(待测)不变,则对所测得的x值无影响,
故答案为:无影响;
(4)2KMnO4 ~5H2C2O4
2 5
aV×10-3mol 0.025×cmol
c=$\frac{5aV×1{0}^{-3}mol}{2×0.025mol}$=0.1aVmol•L-1,
样品中含有草酸的质量为:90g/mol×0.1aVmol/L×0.025L×4=0.9aVg,Wg草酸晶体中含有结晶水的质量为Wg-0.9aVg,
草酸晶体中含有结晶水数目为:x=$\frac{\frac{Wg-0.9aVg}{18g/mol}}{\frac{0.9aVg}{90g/mol}}$=$\frac{50W}{9aV}$-5,
故答案为:0.1aV;$\frac{50W}{9aV}$-5.
点评 本题考查一定物质的量浓度溶液配制、滴定操作中仪器的选用及滴定误差分析,题目难度中等,注意掌握配制一定物质的量浓度的溶液即中和滴定操作的方法,能够根据操作步骤选用仪器、根据操作方法判断滴定误差.

| A. | Cu2+、Na+、SO42-、Cl- | B. | K+、Na+、HCO3-、NO3- | ||
| C. | OH-、Cl-、Ca2+、Na+ | D. | Fe2+、Na+、Cl-、NO3- |
| A. | 标准状况下,22.4L SO3所含的分子数目为NA | |
| B. | 0.2molH2O2催化分解,转移电子数为0.2NA | |
| C. | 0.1mol/L的100mLH2SO3溶液中,含有的离子数约为0.03NA | |
| D. | 6.25 mL1 mol/L浓硫酸与足量铜反应,转移电子数为0.2NA |
| A. | 良好的导电性 | B. | 良好的延展性 | C. | 反应中易失电子 | D. | 良好的导热性 |
| A. | 5.4KJ | B. | 350KJ | C. | 3.5KJ | D. | 8.5KJ |
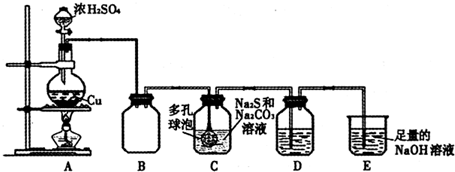
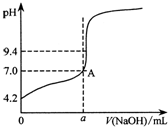 现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作:
现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作: