题目内容
A—H代表中学化学中的常见物质,他们之间的转化关系如下(反应条件已略去)
①A+B→C+D+E ②C+F→G+H ③H+D+E→B
(1)若C、D是两种均能使澄清石灰水变浑浊的气体,且D能使品红溶液褪色,F为淡黄色粉末,则反应①的化学方程式是 ,当有 1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是
1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是  (填2种)。
(填2种)。
(2)若B为黄绿色气体,F为红棕色气体,反应③的部分产物已略去。则反应②的化学方程式是 ,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。
,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。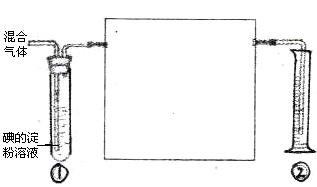
①A+B→C+D+E ②C+F→G+H ③H+D+E→B
(1)若C、D是两种均能使澄清石灰水变浑浊的气体,且D能使品红溶液褪色,F为淡黄色粉末,则反应①的化学方程式是 ,当有
 1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是
1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是  (填2种)。
(填2种)。(2)若B为黄绿色气体,F为红棕色气体,反应③的部分产物已略去。则反应②的化学方程式是
 ,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。
,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。
(1)C+2H2SO4(浓)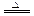 CO2↑+2SO2↑+2H2O 6.02×1023(或NA)
CO2↑+2SO2↑+2H2O 6.02×1023(或NA)
1:2 Cl2、O2、NO2、NH3(写出其中任意2种均可)
(2)H2O+3NO2===NO+2HNO3
2H++ClO-+Cl-===Cl2↑+H2O
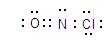
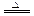 CO2↑+2SO2↑+2H2O 6.02×1023(或NA)
CO2↑+2SO2↑+2H2O 6.02×1023(或NA)1:2 Cl2、O2、NO2、NH3(写出其中任意2种均可)
(2)H2O+3NO2===NO+2HNO3
2H++ClO-+Cl-===Cl2↑+H2O
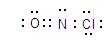
略

练习册系列答案
相关题目
 (5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为 ;该温度下的平衡常数为K= 。
(5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为 ;该温度下的平衡常数为K= 。
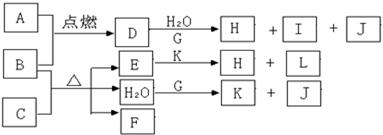
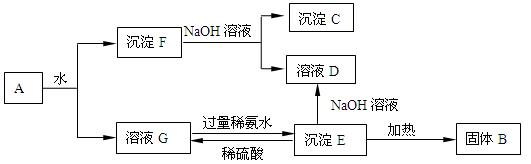

 写出由E转变成F的现象 ;其发生反应的化学方程式________。
写出由E转变成F的现象 ;其发生反应的化学方程式________。