题目内容
(11分)某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图
所示的变化。
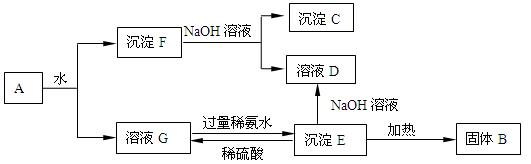
请回答下列问题。
(1)图中涉及分离溶液与沉淀的方法是 。
(2)B、C、D、E 4种物质的化学式为:
B 、C 、D 、E 。
(3)沉淀F与NaOH溶液反应的离子方程式为 。
沉淀E与稀硫酸反应的离子方程式为 。
溶液G与过量稀氨水反应的化学方程式为 。
所示的变化。

请回答下列问题。
(1)图中涉及分离溶液与沉淀的方法是 。
(2)B、C、D、E 4种物质的化学式为:
B 、C 、D 、E 。
(3)沉淀F与NaOH溶液反应的离子方程式为 。
沉淀E与稀硫酸反应的离子方程式为 。
溶液G与过量稀氨水反应的化学方程式为 。
(11分)(1)过滤(1 分)
(2)B: Al2O3 C:Fe2O3 D:NaAlO2 E:Al(OH)3(每空1分)
(3)Al2O3 + 2OH-= 2AlO2- + H2O (2分)
Al(OH)3 + 3H+= Al3+ + 3H2O (2分)
Al2(SO4)3 + 6NH3·H2O = 2 Al(OH)3↓ + 3(NH4)2SO4 (2分)
(2)B: Al2O3 C:Fe2O3 D:NaAlO2 E:Al(OH)3(每空1分)
(3)Al2O3 + 2OH-= 2AlO2- + H2O (2分)
Al(OH)3 + 3H+= Al3+ + 3H2O (2分)
Al2(SO4)3 + 6NH3·H2O = 2 Al(OH)3↓ + 3(NH4)2SO4 (2分)
略

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
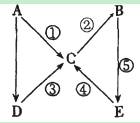
 元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。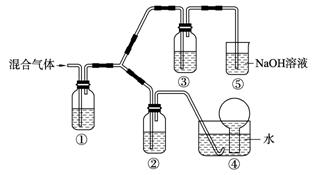
 中学化学中的常见物质,它们之间的转化关系如下图所示,其中A
中学化学中的常见物质,它们之间的转化关系如下图所示,其中A 、D为金属单质,反应过程中
、D为金属单质,反应过程中 生成的水及其他部分产物已略去。
生成的水及其他部分产物已略去。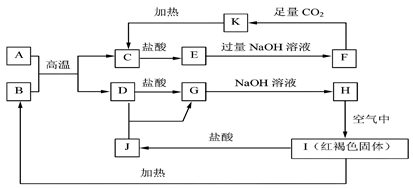
 。
。
 。
。 1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是
1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是  (填2种)。
(填2种)。 ,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。
,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。


 →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
 的四种常见元素W、X、Y、Z,均可形成一种或多种氧化物。其中W、Y的氧化物是导致酸雨的主要物质,X的氧化物既可以和强酸、亦可以和强碱反应,Z则具有砖红色和黑色的两
的四种常见元素W、X、Y、Z,均可形成一种或多种氧化物。其中W、Y的氧化物是导致酸雨的主要物质,X的氧化物既可以和强酸、亦可以和强碱反应,Z则具有砖红色和黑色的两 种氧化物。
种氧化物。 ,用电子式表示其气态氢
,用电子式表示其气态氢 化物 。
化物 。 。
。