题目内容
11.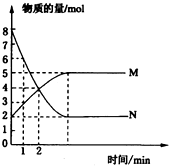 在一定温度下,将两种气体M和N通入容积为2L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示.
在一定温度下,将两种气体M和N通入容积为2L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示.请回答:
(1)该反应的化学反应方程式为2N?M.
(2)0~2min内,用M表示的平均反应速率为0.5mol/(L•min).
(3)平衡时,M与N的物质的量之比为5:2.
(4)不能说明该反应已经达到平衡状态的标志是ac(填选项字母).
a.生成2molM的同时生成1molN b.混合气体的平均相对分子质量保持不变
c.混合气体的密度保持不变 d.N的转化率不变.
分析 (1)根据物质的量的变化与化学计量数呈正比书写化学方程式;
(2)依据反应速率v=$\frac{△c}{△t}$计算得到;
(3)图象分析可知平衡状态MN物质的量不发生变化,M为5mol,N为2mol;
(4)化学平衡的标志是正逆反应速率相同,各组分含量保持不变及其衍生的定量关系;
解答 解:(1)由图象看出反应从开始到平衡,N的物质的量减小,应为反应物,物质的量变化值为8mol-2mol=6mol,
M的物质的量增多,应为是生成物,物质的量的变化值为5mol-2mol=3mol,
根据物质的量的变化与化学计量数呈正比,
则有n(N):n(M)=6mol:3mol=2:1,所以反应的化学方程式为2N?M,
故答案为:2N?M;
(2)0~2min内,M变化物质的量为4mol-2mol=2mol,用M表示的平均反应速率=$\frac{\frac{2mol}{2L}}{2min}$=0.5mol/(L•min);
故答案为:0.5mol/(L•min);
(3)图象分析可知平衡状态MN物质的量不发生变化,M为5mol,N为2mol,平衡时,M与N的物质的量之比为5:2,
故答案为:5:2;
(4)反应是气体体积减小的反应,2N?M;
a.生成2molM的同时生成1molN,不能说明反应达到平衡状态,故a选;
b.气体质量不变,物质的量变化,混合气体的平均相对分子质量保持不变,能说明反应达到平衡状态,故b不选;
c.气体质量和体积都不变,过程中密度始终不变,混合气体的密度保持不变不能说明反应达到平衡状态,故c选;
d.N的转化率不变是平衡标志,故d不选.
故答案为:ac;
点评 本题考查化学反应速率的影响因素以及平衡图象题目,题目难度不大,注意把握图象中曲线的变化特点.

练习册系列答案
相关题目
1.下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置
②金属和石墨导电均为物理变化,电解质溶液导电是学变化
③不能自发进行的氧化还原反应,通过电解的原理有可能实现
④将铜锌原电池用含KCl的盐桥相连时,盐桥中的Cl-会移向正极区
⑤利用电化学原理保护金属主要有两种方法,分别是牺牲阳极的阴极保护法和外加直流电的阴极保护法.
①电解池是将化学能转变成电能的装置
②金属和石墨导电均为物理变化,电解质溶液导电是学变化
③不能自发进行的氧化还原反应,通过电解的原理有可能实现
④将铜锌原电池用含KCl的盐桥相连时,盐桥中的Cl-会移向正极区
⑤利用电化学原理保护金属主要有两种方法,分别是牺牲阳极的阴极保护法和外加直流电的阴极保护法.
| A. | ①②③④ | B. | ④ | C. | ①④⑤ | D. | ②③⑤ |
19.下列说法正确的是( )
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 酸性 HClO4>H2SO4>CH3COOH>H2CO3 |
6.(1)下表是在1.013×105Pa下测得的几种物质的沸点:
从表中数据分析,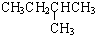 在1.013×105Pa、25℃时的状态是气态(填气态、液态或固态).
在1.013×105Pa、25℃时的状态是气态(填气态、液态或固态).
(2)石油裂解是一个复杂的过程,其产物为混合物.例如:
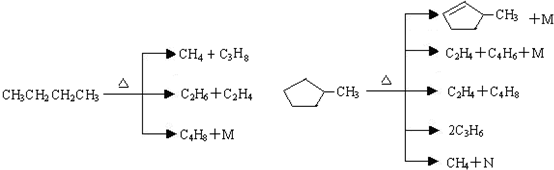
①上述烷烃和环烷烃裂解反应中,产物M的化学式为H2,N的化学式为C5H8.
②下列关于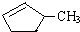 的说法正确的是A.
的说法正确的是A.
A.可用溴水区别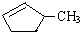 和
和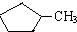
B.等质量的 和
和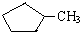 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同
C.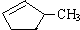 可与水以任意比互溶
可与水以任意比互溶
(3)工业上裂解反应的产物都是气态小分子烷烃和烯烃的混合物,将它们逐一分离的方法是降低温度.
| 结构简式 | 沸点/℃ | 结构简式 | 沸点/℃ |
| CH3CH3 | -88.6 | CH2=CH2 | -103.7 |
| CH3CH2CH3 | -42.2 | CH2=CHCH3 | -47.4 |
| CH3CH2CH2CH3 | -0.5 | CH3CH2CH=CH2 | -6.3 |
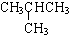 | -11.7 | 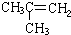 | -6.9 |
| CH3CH2CH2CH2CH3 | 36.1 | CH3CH2CH2CH=CH2 | 30 |
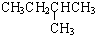 | 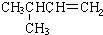 | 20.1 |
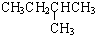 在1.013×105Pa、25℃时的状态是气态(填气态、液态或固态).
在1.013×105Pa、25℃时的状态是气态(填气态、液态或固态).(2)石油裂解是一个复杂的过程,其产物为混合物.例如:

①上述烷烃和环烷烃裂解反应中,产物M的化学式为H2,N的化学式为C5H8.
②下列关于
 的说法正确的是A.
的说法正确的是A.A.可用溴水区别
 和
和
B.等质量的
 和
和 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同C.
 可与水以任意比互溶
可与水以任意比互溶(3)工业上裂解反应的产物都是气态小分子烷烃和烯烃的混合物,将它们逐一分离的方法是降低温度.
3.m g Fe、Fe3O4、Fe2O3的混合物用足量H2还原,固体质量减少4.8g;若将等质量的混合物加入足量的稀硝酸中,产生2.24LNO气体(标准状况下).有关该混合物的下列说法不正确的是( )
| A. | 参加反应的H2和硝酸的物质的量之比为3:1 | |
| B. | 混合物中氧原子的物质的量为0.3mol | |
| C. | 混合物中铁原子的物质的量为0.3mol | |
| D. | 参加反应的硝酸的物质的量为1mol |
15.下列变化涉及的反应类型中,属于加成反应的是( )
| A. | 苯→环已烷 | B. | 乙烯→聚乙烯 | C. | 苯→溴苯 | D. | 甲烷→四氯甲烷 |
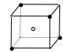 A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子.
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子. H++F-.
H++F-.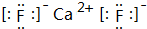 ,其晶体类型为离子晶体.
,其晶体类型为离子晶体.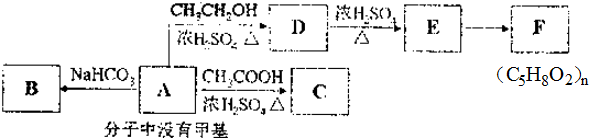
 .
.