题目内容
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体336mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
| A.5.76 | B.2.88 | C.1.44 | D.4.32 |
D
试题分析:发生的反应为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,共收集到336mL的NO气体,反应后溶液中的NO3-的物质的量为NO物质的量的3倍,即n(NO3-)=(336×10-3/22.4)×3=0.045mol,再加稀硫酸发生反应为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,由此可知溶解的Cu的物质的量为NO3-的3/2倍,即m(Cu)=0.045×3/2×64=4.32g.故m1-m2=4.32g,D正确。

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
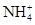
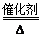 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)