题目内容
以下实验操作错误的是( )
| A、应将浓硝酸存放在棕色玻璃瓶中 |
| B、用托盘天平称量固体的质量时,砝码放在右盘 |
| C、在盛有液溴的试剂瓶里加些水,以防溴挥发 |
| D、少量金属钠保存在水中 |
考点:化学试剂的存放,计量仪器及使用方法
专题:实验评价题
分析:A.硝酸化学性质不稳定,易分解,须存放在棕色试剂瓶中;
B.用托盘天平称量固体药品时,应把砝码放在右盘,药品放在左盘;
C.液溴易挥发,则盛溴的试剂瓶里加少量水以减少溴的挥发;
D.根据金属钠的性质来分析其保存方法,钠性质较活泼,能和氧气、水等物质反应.
B.用托盘天平称量固体药品时,应把砝码放在右盘,药品放在左盘;
C.液溴易挥发,则盛溴的试剂瓶里加少量水以减少溴的挥发;
D.根据金属钠的性质来分析其保存方法,钠性质较活泼,能和氧气、水等物质反应.
解答:
解:A.纯净的硝酸或浓硝酸在常温下见光或受热就会分解,有关反应为:4HNO3
2H2O+4NO2↑+O2↑,在贮存时用棕色试剂瓶可以避免见光,故A正确;
B.用托盘天平称量固体药品时,应把砝码放在右盘,药品放在左盘,先加质量大的砝码,再加质量小的砝码,故B正确;
C.溴易挥发,密度比水大,可用水封以减少溴的挥发,故C正确;
D.钠能和水反应生成氢氧化钠和氢气,所以钠不能保存在水中,钠的密度大于煤油的密度,且钠和煤油不反应,所以把钠放置在煤油中保存而阻止了与氧气和水的反应,故D错误;
故选D.
| ||
B.用托盘天平称量固体药品时,应把砝码放在右盘,药品放在左盘,先加质量大的砝码,再加质量小的砝码,故B正确;
C.溴易挥发,密度比水大,可用水封以减少溴的挥发,故C正确;
D.钠能和水反应生成氢氧化钠和氢气,所以钠不能保存在水中,钠的密度大于煤油的密度,且钠和煤油不反应,所以把钠放置在煤油中保存而阻止了与氧气和水的反应,故D错误;
故选D.
点评:本题主要考查了托盘天平的使用注意事项、药品的保存方法,掌握常见化学实验基本操作的注意事项、以及物质的性质是解题的关键,本题难度不大.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O═Zn(OH)2+Mn2O3,下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、电池正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- |
| C、电池工作时,负极附近pH降低 |
| D、正极是水电离出的H+得到电子 |
现有Fe、CuO、CuCl2、Ca(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有( )
| A、7个 | B、6个 | C、4个 | D、5个 |
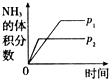
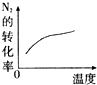
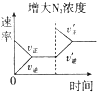
一定条件下将0.1mol N2和0.3mol H2置于密闭容器中发生反应N2+3H2
2NH3.下列关于该反应的说法正确的是( )
| 高温高压 |
| 催化剂 |
| A、最终可生成0.2mol NH3 |
| B、当v正(N2):v正(H2)=1:3时,一定达化学平衡 |
| C、升高温度反应速率增大 |
| D、增大压强反应速率减小 |
短周期元素甲、乙、丙、丁的原子序数依次增大.甲的最高价氧化物与乙的氢化物同时通入水中得到的生成物既可与酸反应又可与碱反应.丙位于IA族,丁原子的核外电子总数是其最外层电子数的3倍,则( )
| A、气态氢化物的稳定性:乙>丁 |
| B、原子半径:甲<乙 |
| C、丙的两种氧化物都是离子化合物 |
| D、甲、乙、丁最高价氧化物对应水化物酸性依次增强 |
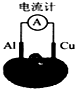 某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )
某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )| A、铝电极是该电池的负极 |
| B、电流由铜片通过导线流向铝片 |
| C、一段时间后,铜片质量会变小 |
| D、该电池将电能转化为了化学能 |