题目内容
对可逆反应N2+3H2
2NH3,下列图象正确的是( )
| ||
| 催化剂 |
A、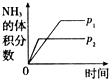 |
B、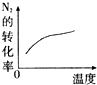 |
C、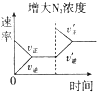 |
D、 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:图示题,化学平衡专题
分析:A、压强增大反应速率增大,平衡向气体体积减小的方向移动,氨气的体积分数增大;
B、升高温度平衡向逆反应方向移动,氮气的转化率降低;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间.
B、升高温度平衡向逆反应方向移动,氮气的转化率降低;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间.
解答:
解:A、压强增大反应速率增大,先到达平衡,故压强P2>P1,增大压强平衡向气体体积减小的方向移动进行,氨气的体积分数增大,图象与实际不相符,故A错误;
B、升高温度平衡向逆反应方向移动,氮气的转化率降低,图象中温度越高氮气的转化率越大,与实际不相符,故B错误;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动,图象与实际相符合,故C正确;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间,图象中没有使用催化剂到达平衡的时间短,与实际不符,故D错误,
故选:C.
B、升高温度平衡向逆反应方向移动,氮气的转化率降低,图象中温度越高氮气的转化率越大,与实际不相符,故B错误;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动,图象与实际相符合,故C正确;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间,图象中没有使用催化剂到达平衡的时间短,与实际不符,故D错误,
故选:C.
点评:本题考查化学平衡图象分析判断,主要是平衡影响因素的分析判断,正确理解平衡移动原理是解题关键,题目难度中等.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、最外层有2个电子的原子都是金属原子 |
| B、除短周期外,其他周期均有18个元素 |
| C、副族元素中没有非金属元素 |
| D、碱金属元素是指IA族的所有元素 |
下列粒子能促进水的电离,且使溶液呈酸性是( )
| A、CO32- |
| B、Fe3+ |
| C、HSO4- |
| D、Cl- |
类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论.下列类推结论正确的是( )
| A、SiH4的熔沸点比CH4高,则PH3的熔沸点比NH3高 |
| B、钠在空气中燃烧生成过氧化钠,则锂在空气中燃烧生成过氧化锂 |
| C、Al(OH)3能溶于NaOH溶液,则Be(OH)2能溶于NaOH溶液 |
| D、甲酸甲酯能发生银镜反应,则乙酸甲酯能发生银镜反应 |
下列说法正确的是( )
| A、硫酸钡难溶于水,其水溶液导电能力极弱,所以硫酸钡是弱电解质 |
| B、CO2溶于水得到的溶液能导电,所以CO2是电解质 |
| C、强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 |
| D、某物质若不是电解质,就一定是非电解质 |
以下实验操作错误的是( )
| A、应将浓硝酸存放在棕色玻璃瓶中 |
| B、用托盘天平称量固体的质量时,砝码放在右盘 |
| C、在盛有液溴的试剂瓶里加些水,以防溴挥发 |
| D、少量金属钠保存在水中 |
下列叙述正确的是( )
| A、两个非金属原子间可能形成离子键 |
| B、非金属原子间不可能形成离子化合物 |
| C、离子化合物中可能有共价键 |
| D、共价化合物中可能有离子键 |
相关城市空气污染的首要污染物是( )
| A、二氧化硫 | B、二氧化氮 |
| C、二氧化碳 | D、可吸入颗粒物 |