题目内容
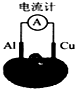 某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )
某兴趣小组用铜片、铝片和番茄(或橘子、白醋)等生活中的材料制作的简易电池如图所示,下列叙述正确的是( )| A、铝电极是该电池的负极 |
| B、电流由铜片通过导线流向铝片 |
| C、一段时间后,铜片质量会变小 |
| D、该电池将电能转化为了化学能 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置能自发的进行氧化还原反应,属于原电池,Al易失电子作负极、Cu作正极,电流从正极沿导线流向负极,据此分析解答.
解答:
解:A.Al易失电子作负极,故A正确;
B.Al易失电子作负极、Cu作正极,电流从正极铜片沿导线流向负极铝片,故B正确;
C.正极上铜不参加反应,所以铜片质量不变,故C错误;
D.该装置是将化学能转化为电能的装置,属于原电池,故D错误;
故选AB.
B.Al易失电子作负极、Cu作正极,电流从正极铜片沿导线流向负极铝片,故B正确;
C.正极上铜不参加反应,所以铜片质量不变,故C错误;
D.该装置是将化学能转化为电能的装置,属于原电池,故D错误;
故选AB.
点评:本题考查了原电池原理,明确原电池和电解池区别是解本题关键,再结合失电子难易程度确定正负极,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
以下实验操作错误的是( )
| A、应将浓硝酸存放在棕色玻璃瓶中 |
| B、用托盘天平称量固体的质量时,砝码放在右盘 |
| C、在盛有液溴的试剂瓶里加些水,以防溴挥发 |
| D、少量金属钠保存在水中 |
下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
| A、Mg(OH)2 |
| B、Al(OH)3 |
| C、SiO2 |
| D、SO2 |
相关城市空气污染的首要污染物是( )
| A、二氧化硫 | B、二氧化氮 |
| C、二氧化碳 | D、可吸入颗粒物 |
某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q kJ/mol(Q>0)达到平衡.缩小容器体积,重新达到平衡,C的浓度比原平衡的浓度大.以下分析正确的是( )
| A、产物B的状态只能为固态或液态 |
| B、平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 |
| C、保持体积不变,向平衡体系中加入B,平衡不可能向逆反应方向移动 |
| D、若开始时向容器中加入1mol B和1mol C,达到平衡时放出热量QkJ |
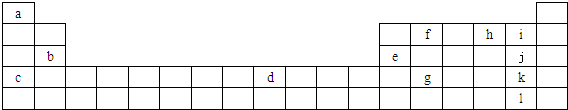
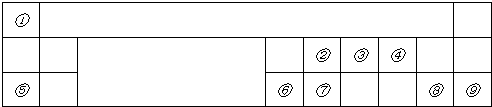
 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中O点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中O点代表氢元素.下列说法中正确的是( )| A、离0点越远的元素原子半径越大 |
| B、虚线相连的元素处于同一族 |
| C、B、C最高价氧化物的水化物不能相互反应 |
| D、A、B组成的化合物中不可能含有共价键 |
下列叙述正确的是( )
| A、标准状况下11.2L CCl4和11.2L CO2分子数相同 |
| B、CH4的摩尔质量为16g |
| C、3.01×1023个SO2分子的质量为32g |
| D、标准状况下,1mol任何物质体积均为22.4L |