题目内容
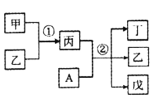
【题目】甲、乙、丙、丁、戊五种物质是中学化学常见的物质,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法正确的是( )
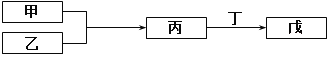
A. 若甲可以与NaOH溶液反应放出H2,则丙一定是两性氧化物
B. 若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊一定是氧化还原反应
C. 若丙、丁混合产生大量白烟,则乙可能会使高锰酸钾溶液褪色
D. 若甲、丙、戊都含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊
【答案】D
【解析】
A.甲为单质,若甲可以与NaOH溶液反应放出H2,则甲为Al或Si,所以丙可能是氧化铝,也可能是二氧化硅,不一定是两性氧化物,故A错误;B.若甲为短周期中最活泼的金属,且戊为碱,则甲为Na,乙为氧气,所以丙可以为氧化钠或过氧化钠,当丙为氧化钠时,丙生成戊不是氧化还原反应,故B错误;C.丙、丁混合产生白烟,则丙、丁可为HCl和NH3或HNO3和NH3等,甲、乙均为单质,则乙可能是氯气、氢气或氮气,都不能使高锰酸钾溶液褪色,故C错误;D.若甲、丙、戊含有同一种元素,例如当甲为S、乙为氧气、丙为二氧化硫、丁为HClO等具有强氧化性的物质、戊为硫酸时,则含S元素的物质中S的化合价由低到高的顺序为甲<丙<戊,故D正确;故选D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目