题目内容
12.下列说法不正确的是( )| A. | 二氧化硫可用作一些食品的杀菌剂 | |
| B. | 明矾[KAl(SO4)2•12H2O]既可用做净水剂,也可用作消毒剂 | |
| C. | 浓硫酸、浓硝酸均具有强氧化性,常温下均可用铝制容器盛放 | |
| D. | NH4HCO3受热易分解放出NH3和CO2,可用作制作糕点时的发酵剂、膨松剂 |
分析 A.二氧化硫有毒,能杀菌消毒;
B.明矾中铝离子能水解生成氢氧化铝胶体,具有能净水,但没有强氧化性;
C.浓硫酸、浓硝酸在常温下能和Al发生钝化现象;
D.碳酸氢铵受热分解生成NH3和CO2,生成的气体在面团里形成大量气泡,使得面包变得松软.
解答 解:A.二氧化硫有毒,能使蛋白质变性而杀菌消毒,常常用在果脯、葡萄酒,故A正确;
B.明矾中铝离子能水解生成氢氧化铝胶体,具有能净水,但没有强氧化性,所以明矾只能作净水剂不能作消毒剂,故B错误;
C.浓硫酸、浓硝酸在常温下能和Al发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以常温下均可用铝制容器盛放浓硫酸、浓硝酸,故C正确;
D.碳酸氢铵受热分解生成NH3和CO2,生成的气体在面团里形成大量气泡,使得面包变得松软,所以可用作制作糕点时的发酵剂、膨松剂,故D正确;
故选B.
点评 本题考查物质的用途,为高频考点,明确物质的性质是解本题关键,性质决定用途而用途体现性质,易错选项是A.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2. 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用.
工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1
下表所列数据是以上反应在不同温度下的化学平衡常数的数值:
(1)Ⅰ、在一密闭容器中发生反应并达到平衡后,保持其他条件不变,对容器升温,此反应的化学反应平衡应逆向移动(填“正向”、“逆向”、“不”)
Ⅱ、某温度下,将1mol CO和4mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1mol/L,则CO的转化率为80%,此时的温度>250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-Q1kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-Q2 kJ/mol
③H2O(g)=H2O(l)△H3=-Q3 kJ/mol
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-(0.5Q1-0.5Q2-2Q3)kJ/mol
(3)某同学依据甲醇燃烧的反应原理,设计如右图所示的电池装置,工作一段时间后,测得溶液的pH将降低(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:CH3OH-6e-+8OH-═CO32-+6H2O.
 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用.工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1
下表所列数据是以上反应在不同温度下的化学平衡常数的数值:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
Ⅱ、某温度下,将1mol CO和4mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1mol/L,则CO的转化率为80%,此时的温度>250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-Q1kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-Q2 kJ/mol
③H2O(g)=H2O(l)△H3=-Q3 kJ/mol
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-(0.5Q1-0.5Q2-2Q3)kJ/mol
(3)某同学依据甲醇燃烧的反应原理,设计如右图所示的电池装置,工作一段时间后,测得溶液的pH将降低(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:CH3OH-6e-+8OH-═CO32-+6H2O.
3.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 再加入10mL pH=11 NaOH溶液,混合液pH=7 | |
| B. | 醋酸的电离程度增大,c(H+)亦增大 | |
| C. | 溶液中导电粒子的数目增加,导电性增强 | |
| D. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•(O{H}^{-})}$不变 |
20.如图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程.
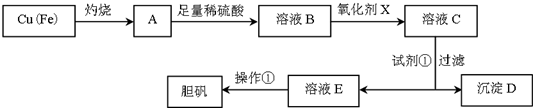
已知:
请回答:
(1)溶液B中含有的阳离子有Fe2+、Fe3+、H+、Cu2+(填离子符号).
(2)下列物质中最适宜作氧化剂X的是b(填字母).a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(4)操作①的名称是蒸发浓缩、冷却结晶.
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是c
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液.实验室保存FeCl2溶液,需加入过量的铁粉,其原因是2Fe3++Fe=3Fe2+(用离子方程式表示).

已知:
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
(1)溶液B中含有的阳离子有Fe2+、Fe3+、H+、Cu2+(填离子符号).
(2)下列物质中最适宜作氧化剂X的是b(填字母).a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(4)操作①的名称是蒸发浓缩、冷却结晶.
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是c
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液.实验室保存FeCl2溶液,需加入过量的铁粉,其原因是2Fe3++Fe=3Fe2+(用离子方程式表示).
7.对于在在标准状况下,22.4LO2中说法是正确的是( )
| A. | 物质的量不是1mol | B. | 含的氧原子个数为1mol | ||
| C. | 质子数是2mol | D. | 氧分子个数为1mol |
17.下列有关实验的叙述中,正确的是( )
| A. | 红热的铁与水蒸气反应可生成氧化铁和氢气 | |
| B. | 将二氧化硫通入到紫色石蕊溶液中,溶液先变红后褪色 | |
| C. | 加热时,可将试管、蒸发皿、坩埚直接在酒精灯焰上加热 | |
| D. | 称量氢氧化钠固体时,应将氢氧化钠固体放在称量纸上称量 |
4.下列各项中,由实验事实能得出相应结论的是( )
| 选项 | 理由 | 结论 |
| A | 相同物质的量浓度溶液的pH: Ca(ClO)2>CH3COONa | 酸性:CH3COOH>HClO |
| B | 同体积相同pH的盐酸和醋酸与相同的锌 反应的速率:醋酸>盐酸 | 酸性:HCl>CH3COOH |
| C | 相同条件下的沸点: H2O>NH3 | 非金属性:O>N |
| D | 相同物质的量得到电子的数目: 稀硝酸>浓硝酸 | 氧化性:稀硝酸>浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
1.有关碱金属的叙述正确的是( )
| A. | 随核电荷数的增加,碱金属单质的熔点逐渐降低,密度逐渐增大 | |
| B. | 碱金属单质的金属性很强,均易与氯气、氧气、氮气等发生反应 | |
| C. | 碳酸铯加热时不能分解为二氧化碳和氧化铯 | |
| D. | 无水硫酸铯的化学式为Cs2SO4,它不易溶于水 |
2.在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
(已知N2(g)+3H2(g)═2NH3(g);△H=-92.4kJ•mol-1),下列说法正确的是( )
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol N2、3mol H2 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
| A. | c1<c2<2c1 | B. | a+b>92.4 | C. | α1+α 2=1 | D. | ρ2=3ρ1 |