题目内容
【题目】常温下.用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对 数值lgc(S2-)与lgc(M2+)关系如下图所示,下列说法正确的是
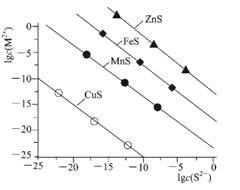
A.室温时.向ZnS悬浊液中加人ZnSO4固体,.Ksp(ZnS)将随之减小
B.Na2S溶液中:c(OH-)<c(H+)+c(HS-)+c(H2S)
C.为除去MnCl2溶液中混有的少量 CuCl2,可加入适量Na2S固体,充分搅拌后过滤
D.向100 mL浓度均为1×10-5mol/L的Fe2+、Zn2+混合溶液中逐滴加入1×10-4mol/LNa2S溶液,Fe2+先沉淀,证明Ksp(FeS)<Ksp(ZnS)
【答案】D
【解析】
试题分析:A、Ksp只受温度的影响,温度不变,Ksp不变,故错误;B、根据质子守恒,c(OH-)=c(H+)+c(HS-)+2c(H2S),因此c(OH-)>c(H+)+c(HS-)+c(H2S),故错误;C、除杂不能引入新杂质,加入Na2S,引入Na+,故错误;D、Fe2+先沉淀出来,说明消耗少量的S2-,就能大于Ksp,说明Ksp((FeS)<Ksp(ZnS),故正确。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
【题目】已知下表中烷烃的某种同分异构体的一氯代物都只有一种结构,依据表中物质的分子式推测表中第六项应该为( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H6 | C5H12 | C8H18 | C17H36 | …… | C53H108 | C80H162 |
A. C22H46 B. C26H54 C. C30H62 D. C32H66