题目内容
工业上合成氨的主要生产过程有:
(1)原料气的制备、净气和压缩。氮气来源于________,氢气来源于________,净化原料气的原因是__________________________________________________________。
(2)氨的合成。在________中进行,反应的最佳条件是_______________________________________________________________。
(3)氨的分离。如将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中通常含体积分数为15%左右的氨气,则出来的混合气体中含H2的体积分数为________,N2的体积分数为________。
(1)原料气的制备、净气和压缩。氮气来源于________,氢气来源于________,净化原料气的原因是__________________________________________________________。
(2)氨的合成。在________中进行,反应的最佳条件是_______________________________________________________________。
(3)氨的分离。如将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中通常含体积分数为15%左右的氨气,则出来的混合气体中含H2的体积分数为________,N2的体积分数为________。
(1)空气 水和碳氢化合物 防止催化剂中毒
(2)合成塔 压强20~50 MPa,温度400~500 ℃,铁触媒作催化剂
(3)63.75% 21.25%
(2)合成塔 压强20~50 MPa,温度400~500 ℃,铁触媒作催化剂
(3)63.75% 21.25%
(3)设起始N2、H2的体积分别为1、3,反应中转化的N2的体积为x,则
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
起始体积 1 3 0
平衡体积 1-x 3-3x 2x
依题意:
 ×100%=15%
×100%=15%
解得:x=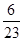
故φ(H2)= ×100%=63.75%
×100%=63.75%
φ(N2)=1-φ(H2)-φ(NH3)=21.25%
N2(g)+3H2(g)
 2NH3(g)
2NH3(g)起始体积 1 3 0
平衡体积 1-x 3-3x 2x
依题意:
 ×100%=15%
×100%=15%解得:x=
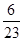
故φ(H2)=
 ×100%=63.75%
×100%=63.75%φ(N2)=1-φ(H2)-φ(NH3)=21.25%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
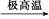 3C+4H2
3C+4H2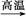 C3H6+H2
C3H6+H2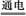 2H2↑+O2↑
2H2↑+O2↑
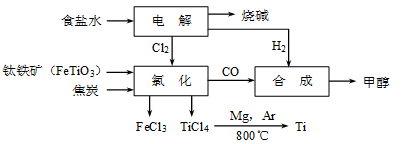
 CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2 mol。
CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2 mol。