��Ŀ����
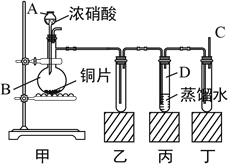
����Ŀ��ijѧУ��ѧѧϰС��Ϊ̽���������������ʣ�����ͼ��ʾװ�ý���ʵ�顣
��ش��������⣺
��1��װ�ü���ʢ��Ũ���������A��������__________����װ���з�����Ӧ�Ļ�ѧ����ʽΪ_________________________��
��2��ʵ������У�װ���ҡ����г��ֵ�����ֱ��ǣ�____________________��____________________��װ�ñ��е��Թ��ڷ�����Ӧ�����ӷ���ʽΪ��_____________________��
��3��ȡ��װ�ñ��е��Թ�D�������еμ�FeSO4��Һ����Һ��Ϊ__________ɫ��Ϊ��֤����Ԫ���ڸ÷�Ӧ�еIJ������____________________________________________________________��
���𰸡� ��Һ©�� Cu+4HNO3(Ũ)=Cu(NO3)2+2NO2��+2H2O ���ɺ���ɫ���� ����ˮ������ɫ���ݣ����Ϸ���Ϊ����ɫ 3NO2+H2O=2H++![]() +NO �� ȡ����������Һ���Թ��У�����KSCN��Һ������ΪѪ��ɫ����֤������Fe3+
+NO �� ȡ����������Һ���Թ��У�����KSCN��Һ������ΪѪ��ɫ����֤������Fe3+
����������1��װ�ü���ʢ��Ũ���������A�������Ƿ�Һ©������ƿ�з���Ũ������ͭƬ��������ԭ��Ӧ����ѧ����ʽΪ��Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O���ʴ�Ϊ����Һ©����Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��
��2��ͭ��Ũ������װ�ü��з�ӦCu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O�����ɺ���ɫ�Ķ����������������װ�ã�����װ�����г��ֵ�����Ϊ���ɺ���ɫ���壻�������������ܽ����װ�ú�ˮ��Ӧ3NO2+H2O�T2H++2NO3-+NO�����ɵ�һ��������Һ���Ϸ��Ŀ�����Ӧ���ɺ���ɫ�Ķ�������������װ�ñ��г��ֵ�����Ϊ����ˮ������ɫ���ݣ����Ϸ���Ϊ����ɫ���ʴ�Ϊ�����ɺ���ɫ���壻����ˮ������ɫ���ݣ����Ϸ���Ϊ����ɫ��3NO2+H2O�T2H++2NO3-+NO��
��3����װ���е�Һ��Ϊ����������ˮ��Ӧ���ɵ����ᣬ������������ԣ������������л�ԭ�ԣ����߷���������ԭ��Ӧ4H++NO3-+3Fe2+=NO+H2O+3Fe3+�������Ӻ���������ӷ�ӦFe3++3SCNFe��SCN��3����Ѫ��ɫ��������֤�������������ӵ����ɣ����Ҫ֤����Ԫ���ڸ÷�Ӧ�еIJ����������Һ�еμ�KSCN��Һ������Һ�Ƿ��ΪѪ��ɫ���ʴ�Ϊ������ȡ����������Һ���Թ��У�����KSCN��Һ������ΪѪ��ɫ����֤������Fe3+��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�