题目内容
【题目】设NA表示阿伏加德罗常数,下列说法正确的是( )
A. 2.4g金属镁变成镁离子时失去的电子数目为0.1NA
B. 常温下,2g氢气所含分子数目为NA
C. 在25℃,![]() 时,11.2L氮气所含的原子数目为NA
时,11.2L氮气所含的原子数目为NA
D. 标准状况下22.4L单质溴所含的分子数为NA
【答案】B
【解析】A. 2.4g金属镁的物质的量是0.1mol,变成镁离子时失去的电子数目为0.2NA,A不正确;B. 常温下,2g氢气的物质的量是1mol,所含分子数目为NA,B正确;C. 在25℃,1.01×105Pa时气体的摩尔体积不是22.4L/mol,11.2L氮气所含的原子数目不是NA,C错误;D. 标准状况下溴是液体,22.4L单质溴所含的分子数不是NA,D错误。答案选B。

练习册系列答案
相关题目
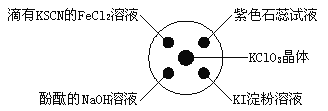
【题目】已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |