题目内容
下列离子方程式中正确的是 ( )
A.工业上粗硅的制备:SiO2+C Si+CO2↑
Si+CO2↑
B.Cu2O与稀H2SO4反应:Cu2O+2H+=2Cu++H2O
C.用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO3-=3Ag++NO↑+2H2O
D .向Mg(HCO3)2溶液中加足量烧碱溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32-
.向Mg(HCO3)2溶液中加足量烧碱溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32-
练习册系列答案
相关题目
18.水及水溶液对生命活动必不可少,下列有关说法正确的是( )
| A. | 向水中加入明矾可以起到净水作用 | |
| B. | 热糖水降低温度后有固体析出,则原热糖水一定是饱和溶液 | |
| C. | 配制溶液时搅拌可以增大溶质的溶解度 | |
| D. | 物质溶于水时不会放出热量 |
4.工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K).
①由表中数据判断该反应的△H<0(填“>”、“=”或“<”);
②某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是df.
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是D.
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是df.
a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平 衡 时 数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.


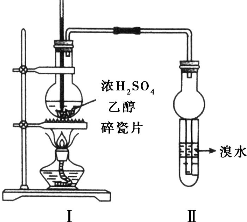 实验室制取乙烯的装置如图所示,试回答:
实验室制取乙烯的装置如图所示,试回答: O = HIO + HCl 不属于氧化还原反应
O = HIO + HCl 不属于氧化还原反应 存在的离子是Na+、OH–
存在的离子是Na+、OH– 溶液均显中性
溶液均显中性
