题目内容
【题目】四甲基氢氧化铵[(CH3)4NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法制备(CH3)4NOH,其工作原理如图所示,下列说法正确的是( )
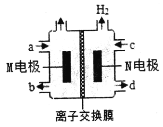
A.M电极的电极反应式为:4OH--4e-=O2↑+2H2O
B.N电极接电源的正极
C.阳离子通过离子交换膜往M电极移动
D.制备18.2g(CH3)4NOH,两极共产生4.48L气体(标准状况)
【答案】D
【解析】
N电极有氢气生成,发生还原反应,故N为阴极,则M为阳极;N极区水放电生成氢气与氢氧根离子,氢氧根离子再与溶液中(CH3)4N+结合生成(CH3)4NOH,M极区是氯离子放电生成氯气,离子交换膜为阳离子交换膜;N极电极反应式为:2(CH3)4N++2H2O+2e=2(CH3)4NOH+H2↑,M极电极反应式为:2Cl2e=Cl2↑。
A.N电极有氢气生成,发生还原反应,故N为阴极,则M为阳极,M极电极反应式为:2Cl2e=Cl2↑,故A错误;
B.N为阴极,连接电源的负极,故B错误;
C.在电解池中,阳离子向阴极移动,N为阴极,所以向N极移动,故C错误;
D.18.2g(CH3)4NOH的物质的量为18.2g÷92g/mol=0.2mol,N极电极反应式为:2(CH3)4N++2H2O+2e=2(CH3)4NOH+H2↑,收集氢气0.1mol,转移电子为0.2mol,M极电极反应式为:2Cl2e=Cl2↑,收集氯气为0.1mol,故标况下两极可得气体体积为:0.2mol×22.4L/mol=4.48L,故D正确;
故答案选D。

练习册系列答案
相关题目