题目内容
【题目】某校化学实验小组,为验证氯单质的氧化性强于硫和氮气,设计了一套实验装置:(部分夹持装置已略去)
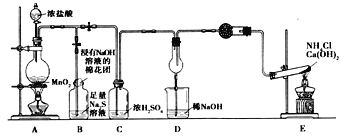
(1)写出A中反应的离子方程式_________。
(2)实验中证明氧化性Cl2>S的实验现象为___________。
(3)D干燥管中产生大量白烟,该反应的化学方程式为 ____________________。
(4)有同学认为从C排出的Cl2可能含有某杂质气体,影响D中现象的判断,该杂质气体是__________,若除去该杂质气体可以用___________溶液。
(5)E装置中反应的化学方程式为_______________________。
【答案】MnO2+4H++2Cl—![]() Mn2++Cl2↑+2H2O B中产生淡黄色沉定或B中溶液变浑浊 8NH3+3Cl2=6NH4Cl+N2 HCl 饱和食盐水 2NH4Cl+Ca(OH)2
Mn2++Cl2↑+2H2O B中产生淡黄色沉定或B中溶液变浑浊 8NH3+3Cl2=6NH4Cl+N2 HCl 饱和食盐水 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
【解析】
(1)此反应装置为浓盐酸和二氧化锰共热制备氯气,以此写出离子方程式;
(2)B中出现黄色浑浊现象,说明有S沉淀生成,氯气的氧化性大于S的氧化性;
(3)装置E为实验室制取氨气的装置,氯气能把氨气氧化生成氮气和氯化氢,氯化氢与氨气反应生成氯化铵,故现象为冒白烟;
(4)浓盐酸易挥发,经过浓硫酸干燥的氯气中仍混有少量氯化氢气体,因此需要在C加一吸收装置,用饱和食盐水除掉氯化氢;
(5)氯化铵和氢氧化钙加热反应生成氨气。
(1)反应装置A为浓盐酸和二氧化锰共热制备氯气的装置,其离子方程式为:MnO2+4H++2Cl—![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)反应制备的氯气通入B之后,B中出现黄色浑浊现象,说明氯气把硫化钠溶液中的硫离子氧化为S单质,离子方程式为Cl2+S2-=S↓+2Cl-;
(3)E装置是制备氨气,氯气能把氨气氧化生成氮气和氯化氢,生成的氯化氢和氨气结合生成氯化铵,从而冒白烟,因此实验的现象是产生大量白烟,反应的方程式是8NH3+3Cl2=6NH4Cl+N2;
(4)盐酸易挥发,生成的氯气中含有氯化氢气体,氯化氢也能直接和氨气结合冒白烟,所以需要在C之前连接一盛有饱和食盐水的装置以除去氯化氢气体;
(5)氯化铵和氢氧化钙固体加热反应生成氨气,反应的化学方程式为2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。