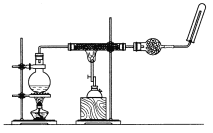
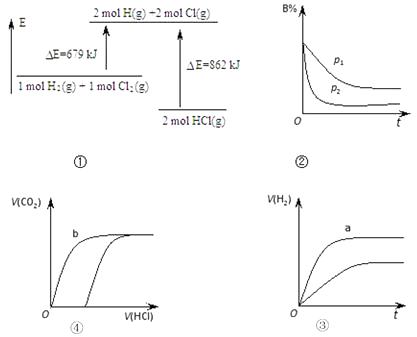
��Ŀ����
����Ŀ����ͼ��ʾ����ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������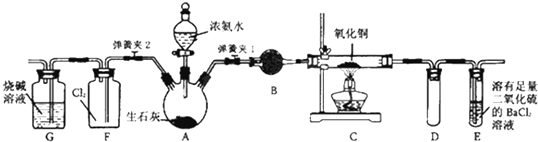
��1������װ��װ�ú���Ҫ����A��Eװ�õ������ԣ����������
�� �� Ȼ����A���쵽E��������ð�����ƿ��ƾ��ƣ�E�е�����ˮ���γ�˵��װ�����������ã�
��2������ƽ���ƶ���ԭ������A����ȡ������ԭ�� ��
��3��װ��B��ʢ���Լ��� ��
��4���رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©����������ȼC���ƾ��ƣ�װ��C�к�ɫ������죬װ��E��
����������E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ ��
��5����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16g����Ӧ����ع�����������2.4g��ͨ������ȷ���ù������ijɷ��� ��
��6���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�У�д���������̵Ļ�ѧ����ʽ �� Ѹ�ٲ���������ԭ���� ��
���𰸡�
��1���رյ��ɼ�2�ͷ�Һ©�����������ɼ�1����E�м�ˮ����û������ĩ��
��2��������ʯ������Ũ��ˮ����ˮ���ų��������ȴ�ʹNH3�ӷ�����Һ��OH��Ũ�����ӣ�����ʹNH3+H2O?NH3?H2O?NH4++OH��������NH3�ƶ����ӿ찱���ݳ�
��3����ʯ��
��4��������ð������������ɫ������2NH3+3CuO ![]() 3Cu+N2��+3H2O
3Cu+N2��+3H2O
��5��Cu2O��Cu
��6��3Cl2+8NH3=N2+6NH4Cl��ʢ�������ļ���ƿ�����������������ɲ��ֹ��壬������ѹ��С��������Һ����
���������⣺��1.����װ��װ�ú���Ҫ����A��Eװ�õ������ԣ�������ǣ����ȹرյ��ɼ�2�ͷ�Һ©�����������ɼ�1����E��װ��ˮ��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƻ��ɿ�˫�֣�E�е�����ˮ���γ�˵��װ�����������ã����Դ��ǣ��رյ��ɼ�2�ͷ�Һ©�����������ɼ�1����E�м�ˮ����û������ĩ�ˣ�
��2.������װ��ͼ��֪��A�н�Ũ��ˮ���뵽��ʯ���У�������ʯ������Ũ��ˮ����ˮ���ų��������ȴ�ʹNH3�ӷ�����Һ��OH��Ũ�����ӣ�����ʹNH3+H2ONH3H2ONH4++OH��������NH3�ƶ����ӿ찱���ݳ������Դ��ǣ�������ʯ������Ũ��ˮ����ˮ���ų��������ȴ�ʹNH3�ӷ�����Һ��OH��Ũ�����ӣ�����ʹNH3+H2ONH3H2ONH4++OH��������NH3�ƶ����ӿ찱���ݳ���
��3.������C��Ӳ���Թܵİ���Ӧ���װ��B�������Ǹ��ﰱ�������ﰱ���ü�ʯ�ң����Դ��ǣ���ʯ�ң�
��4.����Ӧ���β���к���δ��Ӧ�İ�����������E��Һ�����������Ӧ����������泥�����������Ȼ�����Ӧ���������ᱵ���ʻ��а�ɫ������������������Ϊ������ð����������ɫ������װ��C�к�ɫ������죬˵����Cu���ɣ���E���ݳ�Һ����������ֱ�����������˵������������Ϊ������ͬʱ����ˮ��C�з�����Ӧ�Ļ�ѧ����ʽΪ��2NH3+3CuO ![]() 3Cu+N2��+3H2O�����Դ��ǣ�������ð����������ɫ������2NH3+3CuO
3Cu+N2��+3H2O�����Դ��ǣ�������ð����������ɫ������2NH3+3CuO ![]() 3Cu+N2��+3H2O��
3Cu+N2��+3H2O��
��5.��16gCuO�к���CuԪ������Ϊ16g�� ![]() =12.8g��������Ԫ������Ϊ16g��12.8g=3.2g����Ӧ����ع�����������2.4g��ʣ���������Ϊ16g��2.4g=13.6g������12.8g����ʣ����庬��Cu��OԪ�أ���n��Cu��=
=12.8g��������Ԫ������Ϊ16g��12.8g=3.2g����Ӧ����ع�����������2.4g��ʣ���������Ϊ16g��2.4g=13.6g������12.8g����ʣ����庬��Cu��OԪ�أ���n��Cu��= ![]() =0.2mol������OԪ�ص�����Ϊ13.6g��12.8g=0.8g��n��O��=
=0.2mol������OԪ�ص�����Ϊ13.6g��12.8g=0.8g��n��O��= ![]() =0.05mol��n��Cu����n��O��=0.2mol��0.05mol=4��1��2��1����ʣ�����ΪCu2O��Cu�����Դ��ǣ�Cu2O��Cu��
=0.05mol��n��Cu����n��O��=0.2mol��0.05mol=4��1��2��1����ʣ�����ΪCu2O��Cu�����Դ��ǣ�Cu2O��Cu��
��6.��������ǿ�����ԣ�������������N2 �� �������̣�˵�����ɹ��壬�ʻ�����NH4Cl����Ӧ����ʽΪ��3Cl2+8NH3=N2+6NH4Cl��ʢ�������ļ���ƿ�����������������ɲ��ֹ��壬������ѹ��С��������Һ���������Դ��ǣ�3Cl2+8NH3=N2+6NH4Cl��ʢ�������ļ���ƿ�����������������ɲ��ֹ��壬������ѹ��С��������Һ������

 ������ϵ�д�
������ϵ�д�����Ŀ���¶�ΪTʱ����4L�����ܱ������г���2molPCl5����ӦPCl5��g��PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ� ��
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
A.��Ӧ��ǰ50s��ƽ������Ϊv��PCl3��=0.0064mol/��Ls��
B.���������������䣬�����¶ȣ�ƽ��ʱc��PCl3��=0.11mol/L����Ӧ�ġ�H��0
C.��ͬ�¶��£���ʼʱ�������г���4molPCl3��4molCl2 �� �ﵽƽ��ʱ����˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ0.025mol/L
D.��ͬ�¶��£���ʼʱ���������г���2molPCl5��0.40molPCl3��0.40molCl2 �� �ﵽƽ��ǰv��������v���棩