��Ŀ����
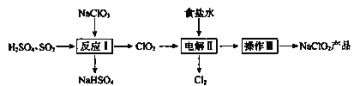
����Ŀ���ܱ���Ϊս�����ʣ��г�ɫ�����ܺ㷺��Ӧ�á���ˮ�ܿ� (��Ҫ�ɷ�ΪCo2O3��CoO��CuO��Fe2O3��CaO��MgO��NiO��SiO2��)Ϊԭ���Ʊ�CoCl2��6H2O�Ĺ���������ͼ��ʾ:

�ش���������:
��.�������
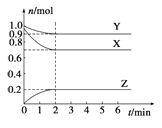
��1���ܵĽ����������ʱ�䡢�¶ȵı仯��ϵ����ͼ��ʾ���ۺϿ��dzɱ���Ӧѡ�����ѹ�������Ϊ______��______������A����Ҫ�ɷ�Ϊ_______��

��2��Co2O3��Ũ���ᷴӦ����CoSO4����ѧ����ʽΪ__________________
��.���������ӡ������������
��3����������������Na2SO4���壬��������ɫ�����������Na2Fe6(SO4)4(OH)12���ӷ���ʽΪ__________________��
��4�����ơ�þ����������NaF����Mg2+ǡ����ȫ����ȥ(����Ũ�ȵ���10-5mol/L)ʱ��c(Ca2+)=__________(��λ��Ч���֣�Ksp(MgF2)=7.4��10-11��Ksp(CaF2)=1.5��10-10��
��5����ͭ����������Na2S2O3��������Ӧ2CuSO4+2Na2S2O3+2H2O=Cu2S��+S��+2Na2SO4+2H2SO4���÷�Ӧ�Ļ�ԭ����Ϊ___________
��.����ȡ�ͷ���ȡ��
��6����ˮ��C���е���Ҫ������Na2SO4��________(д��ѧʽ)��
��7��ʵ���ҳ�ȡ100gԭ��(����11.80%)������ȡʱ�õ�Ũ��Ϊ0.036mol/L��CoCl2��Һ5L��������ģ��ܵIJ���=____(����=������Ԫ������/ԭ���и�Ԫ��������100%)��
���𰸡�90�� 12h SiO2������������� 2Co2O3+4H2SO4��Ũ��![]() 4CoSO4+4H2O+O2�� 2Na++6Fe3++4SO42-+12H2O
4CoSO4+4H2O+O2�� 2Na++6Fe3++4SO42-+12H2O![]() Na2Fe6(SO4)4(OH)12��+12H+ 2.0��10��5mol/L S��Cu2S NiSO4 90%
Na2Fe6(SO4)4(OH)12��+12H+ 2.0��10��5mol/L S��Cu2S NiSO4 90%
��������
��1����ͼ���֪����ѽ����¶�Ϊ90�棬����ѽ���ʱ��Ϊ12h��ˮ�ܿ���Ҫ�ɷ���SiO2����������в����ܽ⣬��������A����Ҫ�ɷ�ΪSiO2��
��2�����ݵ����غ�д���÷�Ӧ�Ļ�ѧ����ʽ��
��3������ԭ���غ�͵���غ��д����Ӧ�����ӷ���ʽΪ��2Na++6Fe3++4SO42-+12H2O![]() Na2Fe6(SO4)4(OH)12��+12H+��
Na2Fe6(SO4)4(OH)12��+12H+��
��4������c(Ca2+)/c(Mg2+)=Ksp��CaF2��/Ksp��MgF2�������c(Ca2+)��
��5������ͭ��CuԪ�صĻ��ϼ���+2�۱�Ϊ+1�ۣ����ϼ۽��ͣ�Na2S2O3��һ����S�Ļ��ϼ۽��ͣ�ת��ΪS��Cu2S�е�S������ԭ������S��Cu2S��
��6���������̵�Ŀ���Լ���Ҫ�ɷ֣��Ƴ�ˮ��C�к��е���Ҫ������Na2SO4��NiSO4��
��7�����ݲ��ʵĹ�ʽ���м��㡣
��1����ͼ��֪�������¶ȣ��ܵĽ��������������60��ʱ����Ч��̫�ͣ�90��ʱ������Ч����100��ʱ������Ч�������ԣ�����100��ʱ�����ɱ�ԶԶ����90��ʱ�����ɱ��������ѽ����¶�Ϊ90�棬����ѽ���ʱ��Ϊ12h��ˮ�ܿ���Ҫ�ɷ���SiO2����������в����ܽ⣬��������A����Ҫ�ɷ�ΪSiO2���ʴ�Ϊ��90�桢12h��SiO2���������������
��2��Co2O3��Ũ���ᷴӦ����CoSO4����֪Co2O3�������������ϼ����߱�������Ԫ��ΪO��-2�۵�����������O2�����ݵ����غ�д���÷�Ӧ�Ļ�ѧ����ʽΪ��
2Co2O3+4H2SO4��Ũ��![]() 4CoSO4+4H2O+O2�����ʴ�Ϊ��2Co2O3+4H2SO4��Ũ��
4CoSO4+4H2O+O2�����ʴ�Ϊ��2Co2O3+4H2SO4��Ũ��![]() 4CoSO4+4H2O+O2����
4CoSO4+4H2O+O2����
��3����������Na2SO4���壬��������ɫ�����������Na2Fe6(SO4)4(OH)12������ԭ���غ�͵���غ��д����Ӧ�����ӷ���ʽΪ��2Na++6Fe3++4SO42-+12H2O![]() Na2Fe6(SO4)4(OH)12��+12H+���ʴ�Ϊ��2Na++6Fe3++4SO42-+12H2O
Na2Fe6(SO4)4(OH)12��+12H+���ʴ�Ϊ��2Na++6Fe3++4SO42-+12H2O![]() Na2Fe6(SO4)4(OH)12��+12H+��
Na2Fe6(SO4)4(OH)12��+12H+��
��4��c(Ca2+)/c(Mg2+)=[c(Ca2+)c2(F��)]/[c(Mg2+)c2(F��)]=Ksp��CaF2��/Ksp��MgF2��=(1.5��10��10)/(7.40��10��11)��c(Mg2+)=10-5mol/L���빫ʽ�����c(Ca2+)=2.0��10��5mol/L���ʴ�Ϊ��2.0��10��5mol/L��
��5����ԭ����������������ԭ�ó������ʣ����ݻ�ѧ��Ӧ����ʽ������ͭ��CuԪ�صĻ��ϼ���+2�۱�Ϊ+1�ۣ����ϼ۽��ͣ�Na2S2O3��һ����S�Ļ��ϼ۽��ͣ�ת��ΪS��Cu2S�е�S������ԭ������S��Cu2S���ʴ�Ϊ��S��Cu2S��
��6���������̵�Ŀ���Լ���Ҫ�ɷ֣��Ƴ�ˮ��C�к��е���Ҫ������Na2SO4��NiSO4���ʴ�Ϊ��NiSO4��
��7�����ݲ��ʵĹ�ʽ���ó��ܵIJ���Ϊ0.036mol/L��5L��59g/mol/��100g��11.80%����100%=90%���ʴ�Ϊ��90%��

����Ŀ����֪��������ĵ���ƽ�ⳣ�����±���ʾ:
���� | ���� | ������ | ̼�� | ������ |
����ƽ�ⳣ��Ka(25��) | 1.75��10-5 | 2.98��10-8 | Ka1=4.3��10-7 Ka2=5.61��10-11 | Ka1=1.54��10-7 Ka2=1.02��10-7 |
�������ӷ���ʽ��ȷ����
A. ������CO2ͨ��NaClO��Һ��:CO2+H2O+2C1O-==CO32-+2HClO
B. ������SO2ͨ��Na2CO3��Һ��:SO2+H2O+2CO32-==SO32-+2HCO3-
C. ������SO2ͨ��Ca(ClO)2��Һ��:SO2+H2O+Ca2++2ClO-==CaSO3��+2HClO
D. ��ͬŨ�ȵ�NaHCO3��Һ��NaHSO3��Һ��������:H++HCO3-==CO2��+H2O