题目内容
14.下列实验报告记录的实验现象正确的是( )| 实验 |  | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
分析 二氧化硫和水反应生成亚硫酸,亚硫酸电离出氢离子而使溶液呈酸性,石蕊试液遇酸变红色;
二氧化硫具有漂白性,能使品红溶液褪色;
二氧化硫具有还原性,能被硝酸钡溶液氧化生成硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;
二氧化硫和碱反应生成亚硫酸根离子,亚硫酸根离子和钡离子反应生成亚硫酸钡沉淀.
解答 解:二氧化硫和水反应生成亚硫酸,亚硫酸电离出氢离子而使溶液呈酸性,石蕊试液遇酸变红色,所以a中试液变红色但不褪色;
二氧化硫能和品红溶液反应生成无色物质而具有漂白性,所以看到的现象是能使品红溶液褪色;
二氧化硫具有还原性,能被硝酸钡溶液氧化生成硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡白色沉淀,所以看到的现象是产生白色沉淀;
二氧化硫和碱反应生成亚硫酸根离子,亚硫酸根离子和钡离子反应生成亚硫酸钡沉淀,所以看到的现象是产生白色沉淀,
故选B.
点评 本题考查二氧化硫的性质,涉及二氧化硫的还原性、水溶液酸性、漂白性等性质,注意二氧化硫不能使酸碱指示剂褪色,注意cd发生的不同点,为易错点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
4.相同物质的量的 Na+、OH-、F- 离子具有相同的( )
| A. | 质量 | B. | 质子数 | C. | 电子数 | D. | 中子数 |
5.下列仪器中,能在酒精灯火焰上直接加热的玻璃仪器是( )
| A. | 试管 | B. | 蒸发皿 | C. | 烧杯 | D. | 蒸馏烧瓶 |
9.体积为V(mL)、密度为ρ(g/cm3)的溶液中,含有摩尔质量为M(g/mol)的溶质m(g),其物质的量浓度为c(mol/L),溶质的质量分数为a%.下列有关关系式不正确的是( )
| A. | m=Vρa% | B. | c=1000ρaM | C. | c=$\frac{1000m}{VM}$ | D. | a%=$\frac{cM}{1000ρ}$×100% |
19.利用碳酸钠晶体(Na2CO3•10H2O)来配制0.5mol•L-1的碳酸钠溶液1000mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A. | 称取碳酸钠晶体100g | |
| B. | 定容时俯视观察刻度线 | |
| C. | 移液时,对用于溶解碳酸钠晶体的烧杯没有进行洗涤 | |
| D. | 定容后,将容量瓶振荡均匀,静置发现液面低于刻度线,于是又加入少量水至刻度线 |
6.下列叙述正确的是( )
| A. | 直径介于1nm~100 nm之间的微粒称为胶体 | |
| B. | 电泳现象可证明胶体带电 | |
| C. | 用盐析法可分离皂化反应后所得的产物 | |
| D. | 用含1mol FeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子 |
3.已知弱酸的电离平衡常数如下表:下列选项正确的是( )
| 弱酸 | H2CO3 | 水杨酸(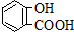 ) ) |
| 电离平衡常数(925℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于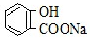 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. |  +2NaHCO3→ +2NaHCO3→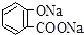 +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. | 水杨酸的第二级电离 Ka2 远小于第一级电离Ka1的原因之一是能形成分子内氢键 |
4.如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程.该方法对H2S的吸收率达99%以上,并可制取H2和S.下列说法正确的是( )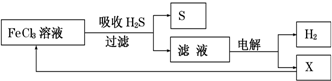

| A. | 吸收H2S的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+ | |
| B. | 电解时选用阴离子交换膜,电解过程中的阳极区反应主要为:2Cl--2e-=Cl2 | |
| C. | 电解过程中若阴极产生2.24L气体,则阳极区产生0.2mol Fe3+ | |
| D. | 实验室可用点燃充分燃烧的方法消除H2S污染 |