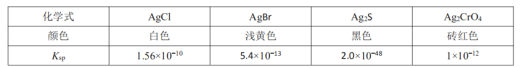
ĖâÄŋÄÚČÝ
ĄūĖâÄŋĄŋČéËáŅĮĖúū§Ėå![]() ĘĮŌŧÖ֚ܚÃĩÄĘģÆ·ĖúĮŋŧŊžÁĢŽŌŨČÜÓÚËŪĢŽÎüĘÕЧđûąČÎÞŧúĖúšÃĢŽŋÉÓÉČéËáÓë
ĘĮŌŧÖ֚ܚÃĩÄĘģÆ·ĖúĮŋŧŊžÁĢŽŌŨČÜÓÚËŪĢŽÎüĘÕЧđûąČÎÞŧúĖúšÃĢŽŋÉÓÉČéËáÓë![]() ·īÓĶÖÆĩÃĢš
·īÓĶÖÆĩÃĢš![]() ĄĢ
ĄĢ
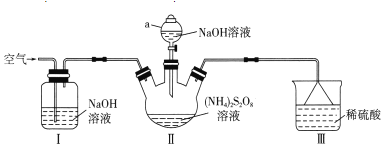
I. ÖÆąļ![]() ĢšŨ°ÖÃČįÏÂÍžËųĘūĢš
ĢšŨ°ÖÃČįÏÂÍžËųĘūĢš
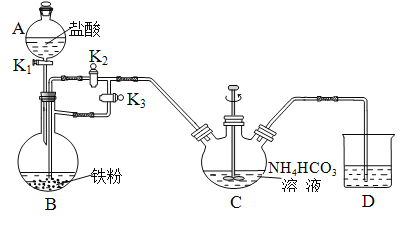
ĒÅBĩÄÃûģÆĘĮ________________ĄĢ
ĒÆĒŲĮåÏīŌĮÆũĢŽžėēéŨ°ÖÃĩÄÆøÃÜÐÔĄĢ
ĒÚĘĩŅéēŲŨũĢšÔÚAÖОÓČëŅÎËáĢŽBÖОÓČëĖú·ÛĄĒCÖОÓČë![]() ČÜŌšĄĢđØąÕŧîČû______(Ėî
ČÜŌšĄĢđØąÕŧîČû______(Ėî![]() ŧō
ŧō![]() ĢŽÏÂÍŽ)īōŋŠŧîČû______ĢŽĩÎČëŨãÁŋŅÎËášóĢŽđØąÕŧîČû
ĢŽÏÂÍŽ)īōŋŠŧîČû______ĢŽĩÎČëŨãÁŋŅÎËášóĢŽđØąÕŧîČû![]() ĢŽŋŠķŊ―Á°čÆũĢŽ·īÓĶŌŧķÎĘąžäšóđØąÕŧîČû______ĄĒīōŋŠŧîČû_______ĄĢ
ĢŽŋŠķŊ―Á°čÆũĢŽ·īÓĶŌŧķÎĘąžäšóđØąÕŧîČû______ĄĒīōŋŠŧîČû_______ĄĢ
CÖзĒÉúĩÄ·īÓĶĩÄĀëŨÓ·―ģĖĘ―ÎŠ_______________________________________ĄĢ
Ēō.ÖÆąļČéËáŅĮĖúū§ĖåĢš―ŦÖÆĩÃĩÄ![]() žÓČëČéËáČÜŌšÖÐĢŽžÓČëÉŲÁŋĖú·ÛĢŽÔÚ
žÓČëČéËáČÜŌšÖÐĢŽžÓČëÉŲÁŋĖú·ÛĢŽÔÚ![]() ÏÂ―Á°čĘđÖŪģä·Ö·īÓĶĄĢČŧšóÔŲžÓČëĘĘÁŋČéËáĄĢ
ÏÂ―Á°čĘđÖŪģä·Ö·īÓĶĄĢČŧšóÔŲžÓČëĘĘÁŋČéËáĄĢ
ĒĮžÓČëÉŲÁŋĖú·ÛĩÄŨũÓÃĘĮ___________________________________ĄĢīÓËųĩÃČÜŌšÖÐŧņĩÃČéËáŅĮĖúū§ĖåËųÐčĩÄĘĩŅéēŲŨũĘĮĢšļôūøŋÕÆøĩÍÎÂÕô·ĒĢŽĀäČī―áū§ĢŽ______ĄĒ______ĄĒļÉÔïĄĢ
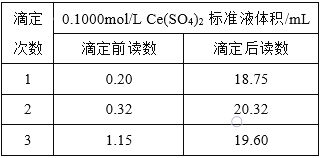
Ēó.ČéËáŅĮĖúū§ĖåīŋķČĩÄēâÁŋĢš
ĒČČôÓÃ![]() ĩÎķĻ·ĻēâķĻŅųÆ·ÖÐ
ĩÎķĻ·ĻēâķĻŅųÆ·ÖÐ![]() ĩÄÁŋ―øķøžÆËãīŋķČĘąĢŽ·ĒÏÖ―áđûŨÜĘĮīóÓÚ
ĩÄÁŋ―øķøžÆËãīŋķČĘąĢŽ·ĒÏÖ―áđûŨÜĘĮīóÓÚ![]() ĢŽÆäÔŌōŋÉÄÜĘĮ_________________________ĄĢ
ĢŽÆäÔŌōŋÉÄÜĘĮ_________________________ĄĢ
ĒÉūēéÔÄÎÄÏŨšóĢŽļÄÓÃ![]() ąęŨžČÜŌšĩÎķĻ―øÐÐēâķĻĄĢ·īÓĶÖÐ
ąęŨžČÜŌšĩÎķĻ―øÐÐēâķĻĄĢ·īÓĶÖÐ![]() ĀëŨÓĩÄŧđÔēúÎïΊ
ĀëŨÓĩÄŧđÔēúÎïΊ![]() ĄĢēâķĻĘąĢŽÏČģÆČĄ
ĄĢēâķĻĘąĢŽÏČģÆČĄ![]() ŅųÆ·ČÜ―âšó―øÐÐąØŌŠīĶĀíĢŽÅäÖÆģÉ250mLČÜŌšĢŽÃŋīÎČĄ
ŅųÆ·ČÜ―âšó―øÐÐąØŌŠīĶĀíĢŽÅäÖÆģÉ250mLČÜŌšĢŽÃŋīÎČĄ![]() ĢŽÓÃ
ĢŽÓÃ![]() ąęŨžČÜŌšĩÎķĻÖÁÖÕĩãĢŽžĮžĘýūÝČįÓŌąíĄĢÔōēúÆ·ÖÐČéËáŅĮĖúū§ĖåĩÄīŋķČΊĢš____________
ąęŨžČÜŌšĩÎķĻÖÁÖÕĩãĢŽžĮžĘýūÝČįÓŌąíĄĢÔōēúÆ·ÖÐČéËáŅĮĖúū§ĖåĩÄīŋķČΊĢš____________![]() ŌÔÖĘÁŋ·ÖĘýąíĘūĢŽČéËáŅĮĖúĘ―ÁŋΊ
ŌÔÖĘÁŋ·ÖĘýąíĘūĢŽČéËáŅĮĖúĘ―ÁŋΊ![]() ĄĢ
ĄĢ
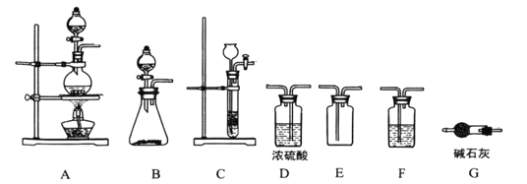
Ąūīð°ļĄŋÕôÁóÉÕÆŋ![]() ŧōūßÖ§ÉÕÆŋ
ŧōūßÖ§ÉÕÆŋ![]()
![]()
![]()
![]()
![]()
![]() ·ĀÖđ
·ĀÖđ![]() ÓëČéËá·īÓĶēúÉúĩÄ
ÓëČéËá·īÓĶēúÉúĩÄ![]() ąŧŅõŧŊ đýÂË ÏīĩÓ ČéËáļųÖÐôĮŧų
ąŧŅõŧŊ đýÂË ÏīĩÓ ČéËáļųÖÐôĮŧų![]() ąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊ
ąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊ ![]() ĄĢ
ĄĢ
Ąū―âÎöĄŋ
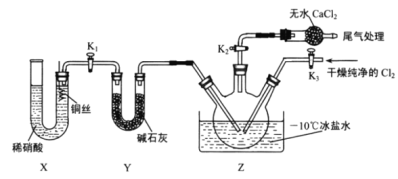
ĒÅÓÉŌĮÆũBĩÄ―áđđĖØÕũĢŽŋÉÖŠBÃûģÆĄĢ
ĒÆÏČ·īÓĶÉúģÉĮâÆøĢŽÅÅģýŨ°ÖÃÄÚŋÕÆøĢŽÔŲĀûÓÃÉúģÉĮâÆøĢŽĘđBŨ°ÖÃÖÐÆøŅđÔöīóĢŽ―ŦBŨ°ÖÃÖÐĩÄÂČŧŊŅĮĖúČÜŌšŅđČëCÖÐĢŽCŨ°ÖÃÖÐ![]() šÍ
šÍ![]() ·ĒÉú·īÓĶĄĢ
·ĒÉú·īÓĶĄĢ
ĒĮ![]() ĀëŨÓŌŨąŧŅõŧŊΊ
ĀëŨÓŌŨąŧŅõŧŊΊ![]() ĀëŨÓĢŽžÓČëFe·ÛĢŽ·ĀÖđ
ĀëŨÓĢŽžÓČëFe·ÛĢŽ·ĀÖđ![]() ĀëŨÓąŧŅõŧŊĢŽīÓËųĩÃČÜŌšÖÐŧņĩÃČéËáŅĮĖúū§ĖåËųÐčĩÄĘĩŅéēŲŨũĘĮļôūøŋÕÆøĩÍÎÂÕô·ĒĄĒĀäČī―áū§ĄĒđýÂËĄĒÏīĩÓĄĒļÉÔïĄĢ
ĀëŨÓąŧŅõŧŊĢŽīÓËųĩÃČÜŌšÖÐŧņĩÃČéËáŅĮĖúū§ĖåËųÐčĩÄĘĩŅéēŲŨũĘĮļôūøŋÕÆøĩÍÎÂÕô·ĒĄĒĀäČī―áū§ĄĒđýÂËĄĒÏīĩÓĄĒļÉÔïĄĢ
ĒČČéËáļųÖКŽÓÐôĮŧųĢŽŋÉŌÔąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊĢŽĩžÖÂÏûšÄļßÃĖËážØĩÄÔöīóĢŽķøžÆËãÖаīŅĮĖúĀëŨÓąŧŅõŧŊĄĢ
ĒÉÏČËãģöÆ―ūųÖĩĢŽÔŲļųūÝ·―ģĖĘ――øÐОÆËãĄĢ
ĒÅÓÉŌĮÆũBĩÄ―áđđĖØÕũĢŽŋÉÖŠBΊÕôÁóÉÕÆŋ(ŧōūßÖ§ÉÕÆŋ)ĢŧđĘīð°ļΊĢšÕôÁóÉÕÆŋ(ŧōūßÖ§ÉÕÆŋ)ĄĢ
ĒÆđØąÕŧîČû![]() ĢŽīōŋŠŧîČû
ĢŽīōŋŠŧîČû![]() ĢŽžÓČëŨãÁŋŅÎËášóĢŽđØąÕŧîČû
ĢŽžÓČëŨãÁŋŅÎËášóĢŽđØąÕŧîČû![]() ĢŽ·īÓĶŌŧķÎĘąžäšóđØąÕŧîČû
ĢŽ·īÓĶŌŧķÎĘąžäšóđØąÕŧîČû![]() ĢŽīōŋŠŧîČû
ĢŽīōŋŠŧîČû![]() ĢŽĀûÓÃÉúģÉĮâÆøĢŽĘđBŨ°ÖÃÖÐÆøŅđÔöīóĢŽ―ŦBŨ°ÖÃÖÐĩÄÂČŧŊŅĮĖúČÜŌšŅđČëCÖÐĢŽCŨ°ÖÃÖÐ
ĢŽĀûÓÃÉúģÉĮâÆøĢŽĘđBŨ°ÖÃÖÐÆøŅđÔöīóĢŽ―ŦBŨ°ÖÃÖÐĩÄÂČŧŊŅĮĖúČÜŌšŅđČëCÖÐĢŽCŨ°ÖÃÖÐ![]() šÍ
šÍ![]() ·ĒÉú·īÓĶĢš
·ĒÉú·īÓĶĢš![]() ĢŽ·īÓĶĀëŨÓ·―ģĖĘ―ÎŠĢš
ĢŽ·īÓĶĀëŨÓ·―ģĖĘ―ÎŠĢš![]() ĢŧđĘīð°ļΊĢš
ĢŧđĘīð°ļΊĢš![]() Ģŧ
Ģŧ![]() Ģŧ
Ģŧ![]() Ģŧ
Ģŧ![]() Ģŧ
Ģŧ![]() ĄĢ
ĄĢ
ĒĮ![]() ĀëŨÓŌŨąŧŅõŧŊΊ
ĀëŨÓŌŨąŧŅõŧŊΊ![]() ĀëŨÓĢŽĘĩŅéÄŋĩÄĘĮÖÆąļČéËáŅĮĖúū§ĖåĢŽžÓČëFe·ÛĢŽ·ĀÖđ
ĀëŨÓĢŽĘĩŅéÄŋĩÄĘĮÖÆąļČéËáŅĮĖúū§ĖåĢŽžÓČëFe·ÛĢŽ·ĀÖđ![]() ĀëŨÓąŧŅõŧŊĢŽīÓËųĩÃČÜŌšÖÐŧņĩÃČéËáŅĮĖúū§ĖåËųÐčĩÄĘĩŅéēŲŨũĘĮļôūøŋÕÆøĩÍÎÂÕô·ĒĄĒĀäČī―áū§ĄĒđýÂËĄĒÏīĩÓĄĒļÉÔïĢŧđĘīð°ļΊĢš·ĀÖđ
ĀëŨÓąŧŅõŧŊĢŽīÓËųĩÃČÜŌšÖÐŧņĩÃČéËáŅĮĖúū§ĖåËųÐčĩÄĘĩŅéēŲŨũĘĮļôūøŋÕÆøĩÍÎÂÕô·ĒĄĒĀäČī―áū§ĄĒđýÂËĄĒÏīĩÓĄĒļÉÔïĢŧđĘīð°ļΊĢš·ĀÖđ![]() ÓëČéËá·īÓĶēúÉúĩÄ
ÓëČéËá·īÓĶēúÉúĩÄ ![]() ąŧŅõŧŊĢŧđýÂËĢŧÏīĩÓĄĢ
ąŧŅõŧŊĢŧđýÂËĢŧÏīĩÓĄĢ
ĒČČéËáļųÖКŽÓÐôĮŧųĢŽŋÉŌÔąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊĢŽĩžÖÂÏûšÄļßÃĖËážØĩÄÔöīóĢŽķøžÆËãÖаīŅĮĖúĀëŨÓąŧŅõŧŊĢŽđĘžÆËãËųĩÃČéËáŅĮĖúĩÄÖĘÁŋÆŦīóĢŽēúÆ·ÖÐČéËáŅĮĖúĩÄÖĘÁŋ·ÖĘýŧáīóÓÚ![]() ĢŧđĘīð°ļΊĢšČéËáļųÖÐôĮŧų
ĢŧđĘīð°ļΊĢšČéËáļųÖÐôĮŧų![]() ąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊĄĢ
ąŧËáÐÔļßÃĖËážØČÜŌšŅõŧŊĄĢ
ĒÉČýīÎÏûšÄ![]() ąęŨžČÜŌšĖåŧý·ÖąðΊ
ąęŨžČÜŌšĖåŧý·ÖąðΊ![]() ĄĒ
ĄĒ![]() ĄĒ
ĄĒ![]() ĢŽĩÚķþīÎÎóēî―ÏīóĢŽÓĶÉáČĨĢŽÔōÏûšÄąęŨžČÜŌšĖåŧýĩÄÆ―ūųÖĩΊ
ĢŽĩÚķþīÎÎóēî―ÏīóĢŽÓĶÉáČĨĢŽÔōÏûšÄąęŨžČÜŌšĖåŧýĩÄÆ―ūųÖĩΊ![]() ĢŽÓÉĢš
ĢŽÓÉĢš![]() ĢŽŋÉÖŠ
ĢŽŋÉÖŠ![]() ČÜŌšÖÐ
ČÜŌšÖÐ![]() ĢŽđĘ250mLšŽÓÐ
ĢŽđĘ250mLšŽÓÐ![]() ĢŽđĘēúÆ·ÖÐČéËáŅĮĖúū§ĖåĩÄÖĘÁŋ·ÖĘýΊ
ĢŽđĘēúÆ·ÖÐČéËáŅĮĖúū§ĖåĩÄÖĘÁŋ·ÖĘýΊ![]() ĢŧđĘīð°ļΊĢš
ĢŧđĘīð°ļΊĢš ![]() ĄĢ
ĄĢ

ĄūĖâÄŋĄŋĀāÍÆ˞ΎĘĮŧŊŅ§―âĖâÖÐģĢÓÃĩÄŌŧÖÖ˞Ύ·―·ĻĢŽÏÂÁÐÓÐđØ·īÓĶ·―ģĖĘ―ĢĻŧōĀëŨÓ·―ģĖĘ―ĢĐĩÄĀāÍÆÕýČ·ĩÄĘĮĢĻĄĄĄĄĢĐ
ŌŅÖŠ | ĀāÍÆ | |
A | ―ŦFežÓČëCuSO4ČÜŌšÖÐĢš Fe + Cu2+ = Cu + Fe2+ | ―ŦNažÓČëĩ―CuSO4ČÜŌšÖÐĢš 2Na + Cu2+ = Cu + 2Na+ |
B | ÏĄÁōËáÓëBa(OH)2ČÜŌš·īÓĶÖÁČÜŌšģĘÖÐÐÔĢš 2H++SO42Đ+Ba2++2OHĐ=BaSO4Ąý+2H2O | NaHSO4ČÜŌšÓëBa(OH)2ČÜŌš·īÓĶģĘÖÐÐÔĢš 2H++SO42Đ+Ba++2OHĐ=BaSO4Ąý+2H2O |
C | ĖúšÍÂČÆø·īÓĶ2Fe+3Cl2 | ĖúšÍĩĨÖĘ·īÓĶ2Fe+3I2 |
D | ÏōCaĢĻClOĢĐ2ČÜŌšÖÐÍĻČëÉŲÁŋCO2Ģš Ca2++2ClOĐ+CO2+H2O=CaCO3Ąý+2HClO | ÏōCaĢĻClOĢĐ2ČÜŌšÖÐÍĻČëÉŲÁŋSO2Ģš Ca2++2ClOĐ+SO2+H2O=CaSO3Ąý+2HClO |
A.AB.BC.CD.D
ĄūĖâÄŋĄŋđĪŌĩÉÏĀûÓÃČíÃĖŋóĢĻÖũŌŠģÉ·ÖΊMnO2ĢŽÍŽĘąšŽÉŲÁŋĖúĄĒÂÁĩČĩÄŧŊšÏÎïĢĐÖÆąļÁōËáÃĖĩÄģĢžûÁũģĖČįÏÂĢš

ēŋ·Ö―ðĘôŅôĀëŨÓŌÔĮâŅõŧŊÎïÐÎĘ―ÍęČŦģÁĩíĘąČÜŌšĩÄpHžûÏÂąíĢš
ģÁĩíÎï | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 10.4 |
ĢĻ1ĢĐŌŧŅõŧŊÃĖÓÃÁōËáËá―þĘą·ĒÉúĩÄÖũŌŠ·īÓĶĩÄĀëŨÓ·―ģĖĘ―ÎŠ____________________ĄĢËá―þšóžÓČëMnO2―ŦČÜŌšÖÐĩÄFe2ĢŦŅõŧŊģÉFe3ĢŦĢŽÆäÄŋĩÄĘĮ___________ĄĢ
ĢĻ2ĢĐÂËÔüAĩÄģÉ·ÖģýMnO2ÍâĢŽŧđÓÐ_______________ĄĢ
ĢĻ3ĢĐMnO2ĘĮÖÆÔėžîÐÔÐŋÃĖĩįģØĩÄŧųąūÔÁÏĢŽ·ÅĩįĘąļšžŦĩÄĩįžŦ·īÓĶĘ―ÎŠ________ĄĢđĪŌĩÉÏŌÔĘŊÄŦΊĩįžŦĩį―âËáŧŊĩÄMnSO4ČÜŌšÉúēúMnO2ĢŽŅôžŦĩÄĩįžŦ·īÓĶĘ―ÎŠ_________ĢŽĩąŌõžŦēúÉú4.48LĢĻąęŋöĢĐÆøĖåĘąĢŽMnO2ĩÄĀíÂÛēúÁŋΊ______gĄĢ
ĢĻ4ĢĐÃĖĩÄČýÖÖÄŅČÜŧŊšÏÎïĩÄČÜķČŧýĢšKsp(MnCO3)Ģ―1.8ĄÁ10Ģ11ĢŽKsp[Mn(OH)2]Ģ―1.9ĄÁ10Ģ13ĢŽKsp(MnS)Ģ―2.0ĄÁ10Ģ13ĢŽÔōÉÏĘöČýÖÖÄŅČÜÎïĩÄąĨšÍČÜŌšÖÐĢŽMn2ĢŦÅĻķČÓÉīóĩ―ÐĄĩÄËģÐōĘĮ_______Ģū_______Ģū_______ĢĻĖîÐīŧŊŅ§Ę―ĢĐĄĢ