题目内容
【题目】ClO2是一种黄绿色或橙黄色的气体,极易溶于水,可用于水的消毒杀菌、水体中Mn2+等重金属清除及烟气的脱硫脱硝。回答下列问题:
(1)将过硫酸钠(Na2S2O8)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,该反应中氧化剂和还原剂的物质的量之比为_____。
(2)将ClO2通入MnSO4溶液,溶液中可检测到Cl-同时有黑色沉淀生成。该反应的离子方程式为__________。
(3)为研究ClO2脱硝的适宜条件,在1L200 mgL-1 ClO2溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,脱硝后N元素以NO3-形式存在,其关系如下图所示:
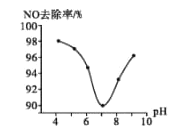
①实验中使用的ClO2溶液的物质的量浓度为______(保留三位有效数字);要使NO的去除率更高,应控制的条件是_________。
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应可生成更强的吸收剂NaClO2,写出碱性条件下NaClO2脱除NO反应的离子方程式:_________。
【答案】1:2 2ClO2+5Mn2++6H2O=5MnO2↓+12H++2Cl- 2.96×10-3 molL-1 控制溶液呈强酸性或强碱性 4NO+3ClO2-+4OH-=4NO3-+3Cl-+2H2O
【解析】
(1)NaClO2中正负化合价代数和为0,该反应中过硫酸钠(Na2S2O8)中S元素的化合价由+7价降低为+6价,过硫酸钠为氧化剂,亚氯酸钠(NaClO2)中Cl的化合价由+3价升高为+4价,亚氯酸钠为还原剂,结合得失电子守恒计算;
(2)将ClO2通入MnSO4溶液中可检测到Cl-同时有黑色MnO2沉淀生成,Cl元素的化合价降低、Mn元素的化合价升高;
(3)①根据n=m/M、c=n/V以及图象分析解答;
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应可生成更强的吸收剂NaClO2,N元素的化合价升高、Cl元素的化合价降低。
(1)将过硫酸钠(Na2S2O8)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价为+3价,该反应中过硫酸钠(Na2S2O8)中S元素的化合价由+7价降低为+6价,过硫酸钠为氧化剂,亚氯酸钠(NaClO2)中Cl的化合价由+3价升高为+4价,亚氯酸钠为还原剂,根据得失电子守恒,过硫酸钠与亚氯酸钠的物质的量之比为1:2;
(2)将ClO2通入MnSO4溶液中可检测到Cl-同时有黑色MnO2沉淀生成,反应的离子方程式为2ClO2+5Mn2++6H2O=5MnO2↓+12H++2Cl-;
(3)①200 mg ClO2的物质的量n(ClO2)=0.2g÷67.5g/mol=0.00296mol,溶液体积为1L,因此ClO2溶液的物质的量浓度为2.96×10-3molL-1,根据图象,要使NO的去除率更高,应该控制溶液呈强酸性或强碱性;
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应可生成更强的吸收剂NaC1O2,在碱性条件下NaClO2脱除NO反应的离子方程式为4NO+3ClO2-+4OH-=4NO3-+3Cl-+2H2O。

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案