题目内容
9.(1)写出下列物质的电子式:H2O2 NH4+
NH4+
(2)写出下列物质的结构式:CH4
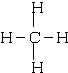 ; CO2O=C=O
; CO2O=C=O下列物质中:
(3)互为同分异构体的有FI
(4)互为同素异形体的有AD
(5)属于同位素的有C
(6)属于同一种物质的有G(填编号)
A.金刚石和石墨 B.${\;}_{19}^{40}K$和${\;}_{20}^{40}$Ca C.${\;}_6^{12}$C和${\;}_6^{14}$C D.O2和O3
E.SO2和SO3 F.CH3CH2OH和CH3OCH3 G.D2O和T2O
H.
 I.
I.
分析 (1)双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
NH4+是多原子构成的阳离子,电子式要加中括号和电荷;
(2)结构式是表示用元素符号和短线表示化合物(或单质)分子中原子的排列和结合方式的式子,一根短线表示一个共用电子,据此分析解答;
(3)分子式相同,结构不同,属于同分异构体;
(4)同种元素构成的不同种单质互为同素异形体;
(5)同种元素的不同种原子互为同位素;
(6)分子式相同,结构相同的为同种物质.
解答 解:(1)双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为:
,NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为: ;故答案为:
;故答案为: ;
; ;
;
(2)甲烷中存在4个碳氢键,甲烷的结构式为: ,故答案为:甲烷中存在4个碳氢键,甲烷的结构式为:
,故答案为:甲烷中存在4个碳氢键,甲烷的结构式为: ;二氧化碳为直线型结构,分子中存在两个碳氧双键,二氧化碳的结构式为:O=C=O;故答案为:
;二氧化碳为直线型结构,分子中存在两个碳氧双键,二氧化碳的结构式为:O=C=O;故答案为: ;O=C=O;
;O=C=O;
A.金刚石和石墨,均属于C原子形成的不同种单质,互为同素异形体;
B.${\;}_{19}^{40}K$和${\;}_{20}^{40}$Ca,质子数不同,属于不同的元素;
C.${\;}_6^{12}$C和${\;}_6^{14}$C,质子数相同,中子数不同,属于同位素;
D.O2和O3,均是由O元素形成的不同种单质,互为同素异形体;
E.SO2和SO3 均属于O和S形成的不同化合物;
F.CH3CH2OH和CH3OCH3 分子式相同,结构不同,属于同分异构体;
G.D2O和T2O,均是由H和O形成的化合物,属于同种物质;
H. ,结构相似,分子组成上相差1个原子团,属于同系物;
,结构相似,分子组成上相差1个原子团,属于同系物;
I. ,分子式相同,结构不同,属于同分异构体,
,分子式相同,结构不同,属于同分异构体,
故答案为:(3)F I; (4)A D; (5)C; (6)G.
点评 本题考查的电子式、结构式的书写,同分异构体、同系物、同素异形体、同位素的概念辨别,难度不大.

| A. | 可溶于水 | B. | 具有较高的熔点 | C. | 水溶液能导电 | D. | 熔融状态能导电 |
| A. | 锌为负极,锌发生氧化反应 | |
| B. | 铜为正极 | |
| C. | 负极发生还原反应,正极发生氧化反应 | |
| D. | 外电路电子流入的一极为正极,电子流出的一极为负极 |
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| ① | Mg Al | 稀盐酸 | 偏向Al |
| ② | Al Cu | 稀盐酸 | 偏向Cu |
| ③ | Al 石墨 | 稀盐酸 | 偏向石墨 |
| ④ | Mg Al | NaOH溶液 | 偏向Mg |
| ⑤ | Al Cu | 浓硝酸 | 偏向Al |
(1)实验①、②的Al所作的电极分别是d(填序号)
a.负极,负极 b.正极,正极
c.负极,正极 d.正极,负极
(2)写出实验③中的电极反应式:铝电极:2Al-6e-═2Al3+,石墨电极:6H++6e-═3H2↑.
(3)对比实验①和②,以及①和④中的电流计指针偏转方向,总结在原电池中电极作正极还是负极受哪些因素影响两个电极的相对活泼性;电解质溶液的酸碱性
(4)解释实验⑤中,电流计指针偏向铝的原因Al钝化作正极,铜易失电子作负极,所以电流计指针偏向铝.

| A. | 该反应是吸热反应 | |
| B. | 断裂1molA-A键和1mol B-B 键放出xkJ能量 | |
| C. | 断裂2molA-B键需要吸收(y-x)kJ的能量 | |
| D. | 1molA2和1molB2的总能量高于2molAB的总能量 |
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>Y>X | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物的水化物的碱性:Y>R>X | |
| D. | 气态氢化物的稳定性:Z>T |
①该反应是一个放热反应
②参加反应的氢气和氧气的总能量高于反应生成的水的总能量
③该反应是一个吸热反应
④参加反应的氢气和氧气的总能量低于反应生成的水的总能量.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |

| A. | 1个乙分子中含有2个A原子 | B. | 摩尔质量关系为:2M (甲)=M (乙)+M (丙) | ||
| C. | 该反应一定属于氧化还原反应 | D. | 该反应类型是分解反应 |