题目内容
1.有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环.其中一种合成路线如下:已知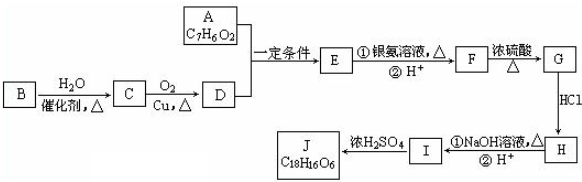
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1.
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平.
③R1-CHO+R2-CH2-CHO一定条件→

回答以下问题:
(1)A中含有的官能团名称是羟基和醛基.
(2)写出有机反应类型B→C加成反应,F→G消去反应.
(3)写出F生成G的化学方程式
 .
.(4)写出J的结构简式
 .
.(5)F的同分异构体有多种,写出所有符合以下要求的F的同分异构体的结构简式
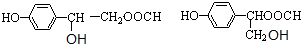 、
、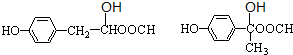 .
.①FeCl3溶液发生显色反应 ②能发生银镜反应 ③苯环上只有两个对位取代基 ④能发生水解反应.
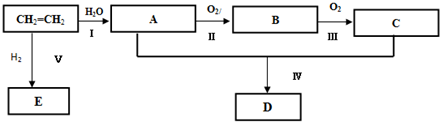
分析 有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平,则B为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生氧化反应得D为CH3CHO,A既能发生银镜反应,又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1,根据A的分子式可知,A为 ,A与D发生题中信息中的反应生成E为
,A与D发生题中信息中的反应生成E为 ,E发生氧化反应生成F为
,E发生氧化反应生成F为 ,F在浓硫酸作用下发生消去反应生成G为
,F在浓硫酸作用下发生消去反应生成G为 ,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为
,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为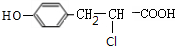 ,H在碱性条件下发生水解生成I为
,H在碱性条件下发生水解生成I为 ,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为
,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为 ,据此答题.
,据此答题.
解答 解:有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平,则B为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生氧化反应得D为CH3CHO,A既能发生银镜反应,又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1,根据A的分子式可知,A为 ,A与D发生题中信息中的反应生成E为
,A与D发生题中信息中的反应生成E为 ,E发生氧化反应生成F为
,E发生氧化反应生成F为 ,F在浓硫酸作用下发生消去反应生成G为
,F在浓硫酸作用下发生消去反应生成G为 ,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为
,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为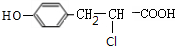 ,H在碱性条件下发生水解生成I为
,H在碱性条件下发生水解生成I为 ,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为
,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为 ,
,
(1)A为 ,A中含有的官能团名称是羟基和醛基,
,A中含有的官能团名称是羟基和醛基,
故答案为:羟基和醛基;
(2)根据上面的分析可知,B→C为加成反应,F→G为消去反应,
故答案为:加成反应;消去反应;
(3)F生成G的化学方程式为 ,
,
故答案为: ;
;
(4)根据上面的分析可知,J的结构简式为 ,
,
故答案为: ;
;
(5)F为 ,根据以下要求①FeCl3溶液发生显色反应,说明有酚羟基,②能发生银镜反应,说明有醛基,③苯环上只有两个对位取代基 ④能发生水解反应,说明有酯基,则符合条件的F的同分异构体的结构简式为
,根据以下要求①FeCl3溶液发生显色反应,说明有酚羟基,②能发生银镜反应,说明有醛基,③苯环上只有两个对位取代基 ④能发生水解反应,说明有酯基,则符合条件的F的同分异构体的结构简式为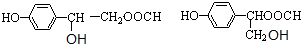 、
、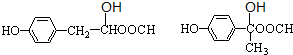 ,
,
故答案为: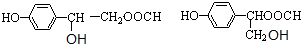 、
、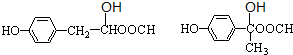 .
.
点评 本题考查有机物的合成,明确合成路线中各物质的推断是解答本题的关键,注意碳链骨架、官能团的变化、反应条件与反应类型的关系即可解答,题目难度中等.

| A. | 78gNa2O2所含有的离子数为3NA | |
| B. | 1mol甲基中含有电子数为10NA | |
| C. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 1molC10H22分子中共价键总数为22NA |
| A. | a和其他3种元素均能形成共价化合物 | |
| B. | 元素的非金属性次序为c>b>a | |
| C. | d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
| A. | 核外电子是分层排布的 | |
| B. | 在化学变化中,活泼金属元素容易失去电子形成阳离子,活泼非金属元素溶液得到电子形成阴离子 | |
| C. | 活泼金属或非金属元素通过电子得失形成离子时,最外层电子趋向于形成类似稀有气体原子的稳定结构 | |
| D. | 原子核外电子绕核做圆周运动 |
| A. | 离子键 | B. | 分子间作用力 | C. | 共价键 | D. | 金属键 |
| A. | 该灰黑色粉末用作抗氧化剂 | B. | 小袋中的原装粉末是Fe2O3 | ||
| C. | 小袋中可能装有活性铁粉 | D. | 该灰黑色粉末不可食用 |
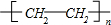 ;反应类型:加聚反应
;反应类型:加聚反应 氯乙烷跟化合物之间的转化如图所示:
氯乙烷跟化合物之间的转化如图所示: