题目内容
13.在单质的晶体中,一定不存在( )| A. | 离子键 | B. | 分子间作用力 | C. | 共价键 | D. | 金属键 |
分析 单质晶体有原子晶体,如Si、金刚石等;有分子晶体,如氢气、臭氧、He等;有金属晶体,如Cu等金属,金属晶体中存在金属键,原子晶体中存在共价键,多原子分子中存在共价键和范德华力、单原子分子中存在范德华力,据此分析解答.
解答 解:单质晶体有原子晶体,如Si、金刚石等;有分子晶体,如氢气、臭氧、He等;有金属晶体,如Cu等金属,金属晶体中存在金属键,原子晶体中存在共价键,多原子分子中存在共价键和范德华力、单原子分子中存在范德华力,离子键是阴阳离子构成的,必须由不同元素构成,所以一定不是单质,故选A.
点评 本题考查单质概念及物质中存在的作用力,侧重考查学生分析判断能力,可以采用举例法分析解答,注意单质中不一定存在化学键,如稀有气体,为易错点.

练习册系列答案
相关题目
19.设NA代表阿伏伽德罗常数的数值,下列说法中正确的是( )
| A. | 1L 1mol•L-1 K2Cr2O2溶液中Cr2O72-的数目为NA | |
| B. | 1mol C60F60分子中碳原子之间共用电子对数目为90NA | |
| C. | 电解精炼铜时,若阴极得到电子数为2NA,则阳极质量减少64g | |
| D. | 标准状况下,2.24L Cl2完全溶于水,转移电子数为0.1NA |
8.分类是化学学习和研究中常用的思维方法,下列关于化学物质和反应类型关系正确的是( )
| A. | 物质$\left\{\begin{array}{l}{混合物}\\{纯净物\left\{\begin{array}{l}{溶液}\\{化合物}\end{array}\right.}\end{array}\right.$ | B. |  | ||
| C. | 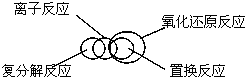 | D. | 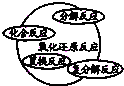 |
5.赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑,对于该反应,下列说法正确的是( )
| A. | 该反应的氧化剂只有Cu2O | |
| B. | Cu既是氧化产物,又是还原产物 | |
| C. | Cu2S在反应中既是氧化剂又是还原剂 | |
| D. | 还原产物与氧化产物的物质的量之比为1:6 |
2.下列化学用语正确的是( )
| A. | 聚丙烯结构简式: | B. | 四氯化碳的电子式为: | ||
| C. | 丙烷分子的比例模型为: | D. | 2-乙基-1,3-丁二烯的键线式: |
3.燃料电池是利用燃料(如H2、CO、CH4等)跟氧气或空气反应,将化学能转化成电能的装置,电解质溶液是强碱.下面关于甲烷燃料电池的说法正确的是( )
| A. | 负极反应为:O2+2H2O+4e═4OH- | |
| B. | 负极反应为:CH4+10OH--8e═CO32-+7H2O | |
| C. | 放电时溶液中的阳离子向负极移动 | |
| D. | 随放电的进行,溶液的pH值不变 |
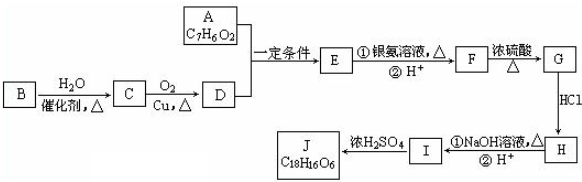

 .
.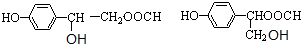 、
、 .
.