题目内容
【题目】(1)1 mol CO2中含有________mol C和________mol O;
(2)1.80 mol CO2中含有________个CO2分子,________个C原子,________个O原子;
(3)3.60 mol CO2中所含CO2分子数与________个H2O分子数目相等,8.40×1026个O3分子的物质的量是________。
【答案】1 2 1.08×1024 1.08×1024 2.17×1024 2.17×1024 1.40×103 mol
【解析】
(1)1molCO2分子中含有1molC和2molO;
(2)由n=![]() ,可知1.80molCO2中含有CO2分子个数为:N(CO2)=n(CO2)×NA=1.80mol×6.02×1023mol-1=1.08×1024;
,可知1.80molCO2中含有CO2分子个数为:N(CO2)=n(CO2)×NA=1.80mol×6.02×1023mol-1=1.08×1024;
该CO2分子中含有1.80mol×6.02×1023mol-1=1.08×1024个C原子,含有1.80mol×6.02×1023mol-1×2=2.17×1024个O原子;
(3)3.60molCO2与3.60molH2O含有相同的分子数:N(H2O)=n(H2O)×NA=3.60mol×6.02×1023mol-1=2.17×1024;
8.40×1026个O3分子的物质的量为:n(O3)=![]() =1.40×103mol。
=1.40×103mol。

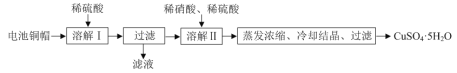
【题目】镍与VA族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓(GaAs),回答下列问题:
(1)基态Ga原子的核外电子排布式为_____,基态As原子核外有_________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为____和+3。砷的电负性比镍____(填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是___________________________________________。
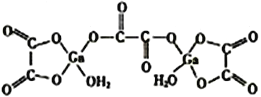
(4)二水合草酸镓的结构如图所示,其中镓原子的配位数为______,草酸根中碳原子的杂化方式为______________。
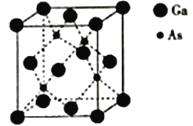
(5)砷化镓熔点为1238℃,立方晶胞结构如图所示,晶胞参数为a=565pm。该晶体的类型为_________,晶体的密度为___________(设NA为阿伏加德罗常数的数值,列出算式即可)g·cm-3。