��Ŀ����
����Ŀ����У������ȤС���ڴ�����ˮ��Ʒʱ������2mol/L���������Ƴ�250mL0.1mol/L��������Һ��
��1����������2mol/L������������_____________��
��2��������ƿ��ʹ�÷����У����в�����ȷ����_______________��
A��ʹ������ƿǰ������Ƿ�©ˮ
B������ƿ��ˮϴ����������õ�ϡHCl��Һ��ϴ
C��������Һʱ������Ͳ��ȡ�õ�����ֱ�ӵ��������У�������ˮ���ӽ��̶���1��2cm�����ý�ͷ�ιܼ�����ˮ���̶���
D���Ǻ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת��Σ�ҡ��
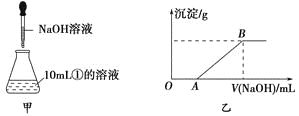
��3������ʱ������������ȷ��������ʱ���ӿ̶��ߣ�������Һ�����ʵ���Ũ��_________��������ƫ��������ƫ��������Ӱ������
���𰸡�12.5mL AD ƫ��
��������
(1)����������Һǰ�����ʵ����ʵ���������㣻
(2)��������ƿ����ȷʹ�÷��������жϣ�
(3)����c=![]() ��ϸ��ӿ̶��ߣ������Һ�����Ӱ������жϡ�
��ϸ��ӿ̶��ߣ������Һ�����Ӱ������жϡ�
(1)������Һǰ�����ʵ����ʵ������䣬����2mol/L����������=![]() =0.0125L=12.5mL���ʴ�Ϊ��12.5mL��
=0.0125L=12.5mL���ʴ�Ϊ��12.5mL��
(2)A������ƿ�ڲ������ӣ�ʹ��ʱ��Ӧ�ȼ���Ƿ�©ˮ��Ȼ��������ˮϴ�Ӹɾ����ɣ���A��ȷ��
B������ƿϴ����������������Һ��ϴ������Ӱ�����Ƶ���Һ��Ũ�ȣ���B����
C������ƿֻ������������Һ������������ƿ��ϡ��Ũ��Һ��Ӧ�����ձ���ϡ�ͣ���C����
D��ҡ��ʱ���Ǻ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת����D��ȷ��
��ѡAD��
(3)������ʱ������������ȷ������ʱ���ӿ̶��ߣ�������Һ�����ƫС����������Һ�����ʵ���Ũ��ƫ�ߣ��ʴ�Ϊ��ƫ�ߡ�

����Ŀ���л���A���������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺
ʵ�鲽�� | ���ͻ�ʵ����� |
��ȡA 9.0 g������ʹ�������������ܶ�����ͬ������H2��45���� | ��ͨ��������գ� |
��1��A����Է�������Ϊ��________�� | |
��2������9.0 g A��������O2�г��ȼ�գ���ʹ��������λ���ͨ��Ũ���ᡢ��ʯ�ң��������߷ֱ�����5.4 g��13.2 g | ��2��A�ķ���ʽΪ��________�� |
��3����ȡA 9.0 g����������NaHCO3��ĩ��Ӧ������2.24 L CO2(��״��)���������������Ʒ�Ӧ������2.24 L H2(��״��) | ��3��д��A�к��еĹ�����____________��________�� |
��4��A�ĺ˴Ź�����������ͼ�� | A�к���4����ԭ�ӡ� |
��4������������A�Ľṹ��ʽΪ________�� | |