��Ŀ����
����Ŀ��������ͭ(Cu2O)��һ����;�㷺�Ĺ����ϣ�ij��������ͭ��ʯ(��CuFeS2��Cu2S��)Ϊԭ����ȡCu2O�Ĺ����������£�
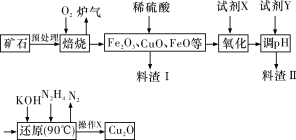
�����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±���
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
��ʼ���� | 7.5 | 2.7 | 4.8 |
��ȫ���� | 9.0 | 3.7 | 6.4 |
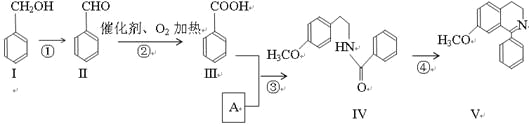
(1)¯���е��к�����ɷ���__________(�ѧʽ)��Cu2S��O2��Ӧʱ���������뻹ԭ�������ʵ���֮��Ϊ__________��
(2)���Լ�X��H2O2��Һ������������Ӧ�����ӷ���ʽΪ____________________����д��H2O2�ĵ���ʽ��__________�����Լ�X��__________ʱ���������ڽ��������ɱ���
(3)�����Լ�Y��pHʱ��pH�ĵ��ط�Χ��__________��
(4)����X����__________��ϴ�ӡ���ɣ����к��ʱҪ������������Ŀ����_________��
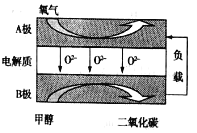
(5)��ͭ��ʯī���缫�����Ũ��ǿ������Һ���Ƶ�����Cu2O��д������������Cu2O�ĵ缫��Ӧʽ��____________________________________��
���𰸡�SO2 2��1 2Fe2����2H����H2O2��2Fe3����2H2O ![]() ���������� 3.7��pH��4.8 ���� ��ֹCu2O���������������� 2Cu��2e����2OH����Cu2O��H2O
���������� 3.7��pH��4.8 ���� ��ֹCu2O���������������� 2Cu��2e����2OH����Cu2O��H2O
��������
��ͭ��ʯ����CuFeS2��Cu2S�ȣ�Ԥ���������������գ�2CuFeS2+4O2![]() Cu2S+3SO2+2FeO��Cu2S+2O2
Cu2S+3SO2+2FeO��Cu2S+2O2![]() 2CuO+SO2������FeO������ΪFe2O3���õ���Ӧ�Ľ���������Ͷ����������壬����ϡ�����ܽ����������õ�����Cu2+��Fe2+��Fe3+��������Һ�������Լ�X��Fe2+����ΪFe3+�������Լ�Y����pH=3.7��4.8������Fe3+�����ˣ�����Һ��KOH��N2H4��ԭ����ӦΪ��4CuSO4+N2H4+8KOH
2CuO+SO2������FeO������ΪFe2O3���õ���Ӧ�Ľ���������Ͷ����������壬����ϡ�����ܽ����������õ�����Cu2+��Fe2+��Fe3+��������Һ�������Լ�X��Fe2+����ΪFe3+�������Լ�Y����pH=3.7��4.8������Fe3+�����ˣ�����Һ��KOH��N2H4��ԭ����ӦΪ��4CuSO4+N2H4+8KOH![]() 2Cu2O+N2��+4K2SO4+6H2O�����ˣ�ϴ�ӡ�����������ɣ��Ƶ�Cu2O��
2Cu2O+N2��+4K2SO4+6H2O�����ˣ�ϴ�ӡ�����������ɣ��Ƶ�Cu2O��
��1���������̿�֪����ʯ�������õ������������SO2��Cu2S��O2������ӦCu2S��2O2![]() 2CuO��SO2��������Ϊ��������ԭ��ΪCu2S���������뻹ԭ�������ʵ���֮��Ϊ2��1���ʴ�Ϊ��SO2��2��1��
2CuO��SO2��������Ϊ��������ԭ��ΪCu2S���������뻹ԭ�������ʵ���֮��Ϊ2��1���ʴ�Ϊ��SO2��2��1��
��2�����Լ�X��H2O2��Һ����Fe2������ΪFe3�������ӷ�Ӧ����ʽΪ2Fe2����2H����H2O2��2Fe3����2H2O��H2O2�ĵ���ʽΪ![]() �������������£�����Ҳ�ɽ�Fe2������ΪFe3����������������۸�Զ���ڹ������⣬�ʿ������������������ʴ�Ϊ��2Fe2����2H����H2O2��2Fe3����2H2O��
�������������£�����Ҳ�ɽ�Fe2������ΪFe3����������������۸�Զ���ڹ������⣬�ʿ������������������ʴ�Ϊ��2Fe2����2H����H2O2��2Fe3����2H2O��![]() �����������
�����������
��3�������Լ�Y��Ŀ���ǵ���pH��ȫ����Fe3������������Cu2�������ݱ������ݿ�֪��pH�ĵ��ط�ΧΪ3.7��pH��4.8���ʴ�Ϊ��3.7��pH��4.8��
��4������XΪ���ˣ�������ϴ�ӡ���ɣ��Ƶ�Cu2O����ΪCu2O���н�ǿ�Ļ�ԭ�ԣ��ڼ����������ױ������������ʺ�ɹ���Ҫ�����������ʴ�Ϊ�����ˣ���ֹCu2O������������������
��5��ͭ��������ʯī�����������Ũ��ǿ������Һ���Ƶ�����Cu2O����������������Ӧ����缫��ӦʽΪ2Cu��2e����2OH����Cu2O��H2O���ʴ�Ϊ��2Cu��2e����2OH��=Cu2O��H2O��

����Ŀ����֪25��ʱ��Ksp(Ag2S)=6.3��10��50��Ksp(AgCl)=1.5��10��16��ij�о���ѧϰС��̽��AgCl��Ag2S����ת����ԭ��
���� | ���� |
��.��NaCl��AgNO3��Һ��� | ������ɫ���� |
��.�����ù�Һ������м�Na2S��Һ | ������Ϊ��ɫ |
��.�˳���ɫ����������NaCl��Һ | �ڿ����з��ýϳ�ʱ�������Ϊ���ɫ |
(1)���еİ�ɫ������__��
(2)������˵��������ڵ����ӷ���ʽ��__��
(3)�˳�����������ɫ�������Ʋ⺬��AgCl����ŨHNO3�ܽ⣬��������ɫ���壬���������ܽ⣬���˵õ���ҺX�Ͱ�ɫ����Y��
��.��X�еμ�Ba(NO3)2��Һ��������ɫ����
��.��Y�еμ�KI��Һ��������ɫ����
���ɢ��жϣ���ҺX�б������������__��
���ɢ�������ȷ�ϲ���������ɫ��������AgCl����һ�ֳ���__��
(4)��ѧ��ͨ�����¶���ʵ��ȷ���˲���������ɫ����������ԭ����NaCl�����£����������к�ɫ����������
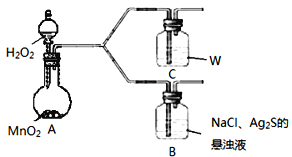
���� | B��һ��ʱ��������ɫ���� |
C��һ��ʱ��������Ա仯 |
��A�����������___��
��C��ʢ�ŵ�����W��__��
�۸�ͬѧ��ΪB�в��������ķ�Ӧ���£��벹����������__
2Ag2S+__+__+2H2O=4AgCl+__+4NaOH
�ܴ��ܽ�ƽ���ƶ��ĽǶȣ�����B��NaCl������__��
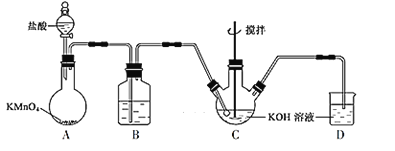
����Ŀ���ס������������ܱ������о�������Ӧ��C(s)��2H2O(g)=CO2(g)��2H2(g)��H��0���й�ʵ���������±���ʾ��
���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ƽ�ⳣ�� | |
C(s) | H2O(g) | H2(g) | ||||
�� | 2 | T1 | 2.0 | 4.0 | 3.2 | K1 |
�� | 1 | T2 | 1.0 | 2.0 | 1.2 | K2 |
����˵����ȷ����(����)
A.K1��12.8
B.T1��T2
C.T1 ��ʱ����������ٳ���0.1 mol H2O(g)����ƽ�������ƶ���CO2(g)�������������
D.��T2�¶��£���2 L�����ܱ������г���1.0 mol CO2��2.0 mol H2����ƽ��ʱ��CO2��ת���ʴ���40%