��Ŀ����
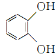
����Ŀ����ˮ�����Ǻϳ����������Ȼ�������Ҫ����,ij�����V�ϳ�·������:
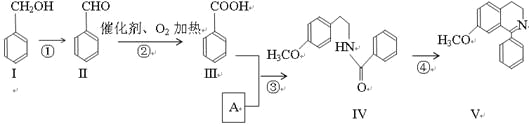
��1�����к��������ŵ�����___________��
��2����Ӧ�ڵĻ�ѧ����ʽ__________________________________��
��3����͢���Ũ���������ʱ��Ӧ�Ļ�ѧ����ʽ______________��
��4������˵����ȷ����___��
A����͢������ڷ����� B�����ܷ���������Ӧ
C��������4molH2�����ӳɷ�Ӧ D����Ӧ������������Ӧ
��5��A�Ľṹ��ʽ___��
��6�������Ϊͬ���칹��,����FeCl3������ɫ��Ӧ,�䱽���ϵ�һ�ȴ���ֻ��2�֡�д���������������Ģ��Ľṹ��ʽ___________��
��7��һ��������,�������(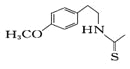 )Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ,���Ļ�������Ľṹ��ʽ____��
)Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ,���Ļ�������Ľṹ��ʽ____��
���𰸡�ȩ�� 2C6H5CHO + O2![]() 2C6H5COOH C6H5CH2OH + C6H5COOH
2C6H5COOH C6H5CH2OH + C6H5COOH![]() C6H5COOCH2C6H5 + H2O B
C6H5COOCH2C6H5 + H2O B ![]()
![]()
![]()
��������
��1�������л���Ľṹ��ʽ���жϢ��к��������ŵ�����ȩ����
��2����Ӧ����ȩ����������Ӧת��Ϊ�Ȼ�����Ӧ�Ļ�ѧ����ʽΪ2C6H5CHO + O2![]() 2C6H5COOH��
2C6H5COOH��
��3����͢���Ũ���������ʱ����������Ӧ����Ӧ�Ļ�ѧ����ʽΪC6H5CH2OH + C6H5COOH![]() C6H5COOCH2C6H5 + H2O��
C6H5COOCH2C6H5 + H2O��
��4�� A.���б�����̼�⻯�����Ƿ����������͢��������ڷ�������A����B��������к���ȩ�����ܷ���������Ӧ��B��ȷ��C��ȩ���ͱ������������������ӳɷ�Ӧ��1mol������4molH2�����ӳɷ�Ӧ�����ڲ���ȷ���л�������ʵ��������ܼ����������������ʵ�����C����ȷ��D����Ӧ�����Ȼ��백����ȡ����Ӧ��������������Ӧ��D����ѡB��
��5�� ��Ӧ�����Ȼ��백����ȡ����Ӧ������ݻ�������Ľṹ��ʽ��֪A�Ľṹ��ʽΪ![]() ��
��
��6�� �����Ϊͬ���칹�壬����FeCl3������ɫ��Ӧ��˵�����з��ǻ����䱽���ϵ�һ�ȴ���ֻ��2�֣�˵�������ϵ���ԭ�ӷ�Ϊ���࣬���������������Ģ��Ľṹ��ʽ![]() ��
��
��7�� һ��������,�������( )Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ�������ת����ϵͼ��֪����Ӧ�л���ˮ���ɣ�����ڻ�����������ķ�Ӧ��Ӧ�û���H2S���ɣ����Ԣ��Ļ�������Ľṹ��ʽΪ
)Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ�������ת����ϵͼ��֪����Ӧ�л���ˮ���ɣ�����ڻ�����������ķ�Ӧ��Ӧ�û���H2S���ɣ����Ԣ��Ļ�������Ľṹ��ʽΪ![]() ��
��

����Ŀ��ij�¶��£���Ӧ��2A��g��B��g��+C��g����ƽ�ⳣ��Ϊ1�����ݻ�Ϊ2L���ܱ������м���A��g����20sʱ��ø���ֵ����ʵ������±�������˵����ȷ���ǣ� ��
���� | A��g�� | B��g�� | C��g�� |
���ʵ���/mol | 1.2 | 0.6 | 0.6 |
A.��Ӧǰ20s�ڵ�ƽ����Ӧ����Ϊv��A��=0.6molL-1s-1
B.20sʱ������Ӧ���ʴ����淴Ӧ����
C.�ﵽƽ��ʱ��A��g����ת����Ϊ100%
D.�������¶�ƽ�ⳣ����Ϊ2����Ӧ����H��0
����Ŀ��FeCl2��һ�ֳ��õĻ�ԭ����ýȾ����ij��ѧʵ��С����ʵ���������������ַ������Ʊ���ˮFeCl2���й����ʵ��������£�
| C6H5Cl(�ȱ��� | C6H4Cl2(���ȱ��� | FeCl3 | FeCl2 |
�ܽ��� | ������ˮ�������ڱ����Ҵ� | ������C6H5Cl��C6H4Cl2������ �������Ҵ�������ˮ | ||
�۵�/�� | -45 | 53 | ������ | |
�е�/�� | 132 | 173 | ||
(1)��H2��ԭ��ˮFeCl3��ȡFeCl2���й�װ�����£�
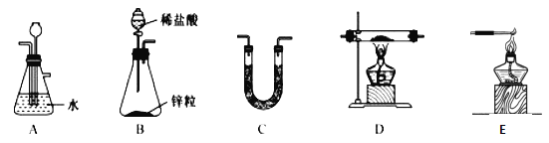
��H2��ԭ��ˮFeCl3��ȡFeCl2�Ļ�ѧ����ʽΪ_____________��
�ڰ����������ҵķ�����������������˳��Ϊ_________������ĸ��װ�ÿɶ��ʹ�ã���C��ʢ�ŵ��Լ���_____________��
�۸��Ʊ�װ�õ�ȱ��Ϊ________________��
(2)���÷�Ӧ2FeCl3+C6H5Cl��2FeCl2+C6H4Cl2+HCl������ȡ��ˮFeCl2���ⶨFeCl3��ת���ʡ�����ͼװ�ã���������ƿ�з���32.5g��ˮ�Ȼ����������ȱ������Ʒ�Ӧ�¶���һ����Χ����3h����ȴ�������ᴿ�õ��ֲ�Ʒ��
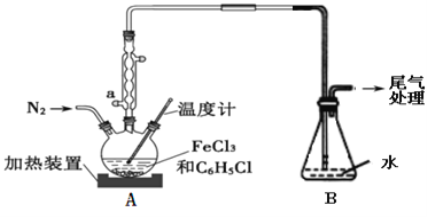
������a��������__________��
�ڷ�Ӧ��������ȴʵ��װ��A����������ƿ�����ʵ����������ˡ�ϴ�ӡ�����õ��ֲ�Ʒ��ϴ�����õ��Լ�������____��������Һ��C6H5C1�IJ���������______��
�۷�Ӧ����ƿ����Һ���250mL����ȡ25.00mL������Һ����0.40mol/LNaOH��Һ�ζ����յ�ʱ����NaOH��ҺΪ19.60 mL�����Ȼ�����ת����Ϊ__________��
��Ϊ�˼���ʵ��������ȡ��ˮFeCl2������Ӧ��ȡ�Ĵ�ʩ�У�________��д��һ�㼴�ɣ���
����Ŀ��������ͭ(Cu2O)��һ����;�㷺�Ĺ����ϣ�ij��������ͭ��ʯ(��CuFeS2��Cu2S��)Ϊԭ����ȡCu2O�Ĺ����������£�
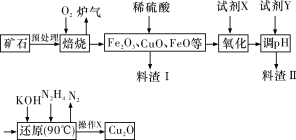
�����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±���
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
��ʼ���� | 7.5 | 2.7 | 4.8 |
��ȫ���� | 9.0 | 3.7 | 6.4 |
(1)¯���е��к�����ɷ���__________(�ѧʽ)��Cu2S��O2��Ӧʱ���������뻹ԭ�������ʵ���֮��Ϊ__________��
(2)���Լ�X��H2O2��Һ������������Ӧ�����ӷ���ʽΪ____________________����д��H2O2�ĵ���ʽ��__________�����Լ�X��__________ʱ���������ڽ��������ɱ���
(3)�����Լ�Y��pHʱ��pH�ĵ��ط�Χ��__________��
(4)����X����__________��ϴ�ӡ���ɣ����к��ʱҪ������������Ŀ����_________��
(5)��ͭ��ʯī���缫�����Ũ��ǿ������Һ���Ƶ�����Cu2O��д������������Cu2O�ĵ缫��Ӧʽ��____________________________________��