题目内容
【题目】在固定容积的密闭容器中进行如下反应:2SO2(g)+O2(g)![]() 2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
A.SO2、O2分别为0.4mol/L、0.3mol/L
B.O2为0.05mol/L
C.SO2、SO3浓度均为0.15mol/L
D.SO2为0.24mol/L、SO3为0.16mol/L
【答案】D
【解析】
A.SO2和O2的浓度增大,说明反应向逆反应方向进行建立平衡,根据硫原子的守恒当SO2的浓度为0.4mol/L时,则SO3的浓度为0,而可逆反应不能进行彻底,即无论进行多长时间,SO3的浓度均不可能为0,故A错误;
B.O2的浓度减小,说明反应向正反应方向进行建立平衡,若SO2完全反应,则消耗氧气的浓度为0.1 mol/L,剩余氧气浓度为0.1 mol/L,实际剩余氧气浓度为0.05mol/L小于0.1mol/L,故B错误;
C.反应物、生产物的浓度不可能同时减小,一个减小,另一个一定增大,故C错误;
D.SO2的浓度增大,说明该反应向正反应方向进行建立平衡,根据反应中的硫原子的守恒,SO2和SO3浓度和一定为0.4mol/L,而现SO2为0.24mol/L,SO3为0.16mol/L,满足硫原子的守恒,故D正确;
故选D。

 53随堂测系列答案
53随堂测系列答案【题目】在2L密闭容器内,800℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为________。
(2)如图中表示O2变化曲线的是________,用O2表示从0~2s内该反应的平均速率v=________。
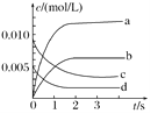
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内气体总质量保持不变
c.v逆(NO)=2v正(O2) d.容器内气体密度保持不变