题目内容
2.下列化学性质中,烷烃不具备的是( )| A. | 可以在空气中燃烧 | |
| B. | 与氯气发生取代反应 | |
| C. | 不能使高锰酸钾溶液褪色 | |
| D. | 可以与溴水中的溴反应而使溴水褪色 |
分析 烷烃中所有键都是单键,烷烃化学性质稳定,不与强酸、强碱、强氧化剂发生反应,但是烷烃中含有C、H两种元素,能够燃烧,且在光照条件下能够发生取代反应,不能与溴水发生反应.
解答 解:A.烷烃中中含有C、H元素,所以烷烃具有“可以在空气中燃烧”的化学性质,故A不选;
B.烷烃的特征反应为取代反应,在光照条件下烷烃能够与氯气发生取代反应,故B不选;
C.烷烃分子中不存在不饱和键,不能使酸性高锰酸钾溶液褪色,故C不选;
D.烷烃为饱和烃,分子中不存在不饱和键,其化学性质稳定,不能与溴水反应而使溴水褪色,故D选;
故选D.
点评 本题考查了烷烃的化学性质,注重了基础知识的考查,难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
12.蛋白质发生的下列过程中,可逆的是( )
| A. | 加入浓硫酸 | B. | 煮熟 | C. | 变性 | D. | 盐析 |
17.下列比较判断不正确的是( )
| A. | 酸性:HClO4>H2SO4 | B. | 碱性:KOH>NaOH | ||
| C. | 半径:S>Cl | D. | 熔点:Na>Li |
7.下列气体中,无色无味的是( )
| A. | SO2 | B. | NO2 | C. | Cl2 | D. | N2 |
14.在一定温度下,将1molCO和1mol水蒸气放入一容积固定的密闭容器中,反应H2O(g)+CO(g)?CO2(g)+H2(g)平衡后,得到0.6molCO2,再通入0.4mol水蒸气,达到平衡后,CO2的物质的量可能为( )
| A. | 1.0mol | B. | 0.7mol | C. | 0.6mol | D. | 0.4mol |
11.铜及其化合物在工农业生产及日常生活中应用非常广泛.某学习小组用粗铜(含杂质铁)制备氧化铜晶体(CuCl2•2H2O)的流程如下.
粗铜$\stackrel{Cl_{2}}{→}$固体$\stackrel{加稀盐酸溶液}{→}$溶液Ⅰ$\stackrel{调节溶液pH}{→}$
已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液Ⅰ之所以要调节溶液pH,目的是除去Fe3+且不引人杂质.调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶、过滤(填操作名称)、洗涤干燥.
(3)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不参与反应),实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2Cu↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为VmL.(已知:I2+2S2O32-═2I-+S4O62-)则该样品中CuCl2•2H2O的质量分数为$\frac{1.71cV}{m}$×100%(用含m,c,V的代数式表示,不用化简).如果达到滴定终点时,仰视滴定管读数将使测定结果偏高(填“偏高”、“偏低”或“无影响”).
(4)已知热化学方程式:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1;
2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1.则由辉铜矿(Cu2S)制取铜的热化学方程式为3Cu2S(s)+3O2(g)=6Cu(s)+3SO2(g),故△H=-652.2kJ•mol-1.
粗铜$\stackrel{Cl_{2}}{→}$固体$\stackrel{加稀盐酸溶液}{→}$溶液Ⅰ$\stackrel{调节溶液pH}{→}$

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
(1)溶液Ⅰ之所以要调节溶液pH,目的是除去Fe3+且不引人杂质.调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶、过滤(填操作名称)、洗涤干燥.
(3)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不参与反应),实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2Cu↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为VmL.(已知:I2+2S2O32-═2I-+S4O62-)则该样品中CuCl2•2H2O的质量分数为$\frac{1.71cV}{m}$×100%(用含m,c,V的代数式表示,不用化简).如果达到滴定终点时,仰视滴定管读数将使测定结果偏高(填“偏高”、“偏低”或“无影响”).
(4)已知热化学方程式:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1;
2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1.则由辉铜矿(Cu2S)制取铜的热化学方程式为3Cu2S(s)+3O2(g)=6Cu(s)+3SO2(g),故△H=-652.2kJ•mol-1.
12.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式不正确的是( )
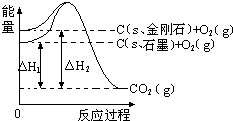

| A. | 石墨和金刚石的转化是化学变化 | |
| B. | 石墨的稳定性强于金刚石 | |
| C. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| D. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
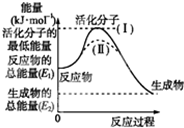 请认真观察图,然后回答问题:
请认真观察图,然后回答问题: