题目内容
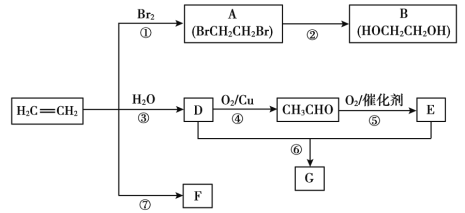
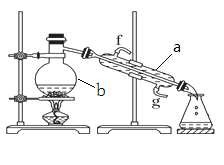
【题目】海洋中有丰富的资源,如图为海水资源利用的部分过程。
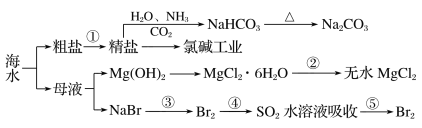
下列有关说法正确的是( )
A.用澄清石灰水可鉴别NaHCO3和Na2CO3
B.第③步和第⑤步均发生了氧化还原反应
C.在第③④⑤步中溴元素均被氧化
D.工业上通过电解饱和MgCl2溶液制取金属镁
【答案】B
【解析】
A. Ca(OH)2与NaHCO3和Na2CO3都能反应生成CaCO3沉淀,所以不能用澄清石灰水鉴别NaHCO3和Na2CO3,A错误;
B. 第③步反应为Cl2+2Br-=2Cl-+Br2,第⑤步反应为5Br-+BrO3-+6H+=3Br2+3H2O,均发生了氧化还原反应,B正确;
C.第④步反应为Br2+SO2+2H2O=2HBr+H2SO4,溴元素被还原,C错误;
D. 工业上通过电解熔融MgCl2制取金属镁,电解氯化镁溶液得不到镁,D错误;
故选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目