��Ŀ����
����Ŀ����������������Դ�����ˮ�����Ⱦ�ǻ�����������Ҫ�о����⡣
(1)��֪��Ӧ8NH3+6NO2=7N2+12H2O���������������ͻ�ԭ���������֮��Ϊ________��
(2)ˮ���й�������(��NH3��ʾ)�ᵼ��ˮ�帻Ӫ������
���ô������Ƴ�ȥ������ԭ������ͼ��ʾ��д����ͼʾ���ܷ�Ӧ��ѧ����ʽ��________��
�÷�Ӧ������¶ȣ��¶ȹ���ʱ����ȥ���ʽ��͵�ԭ����________��
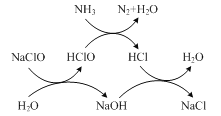
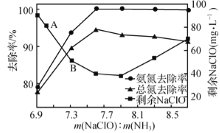
��ȡһ�����ĺ�������ˮ���ı�������������������Ӧһ��ʱ�����Һ�а���ȥ���ʡ��ܵ�(��Һ�����п����Եĺ����������е�Ԫ�ص�����)ȥ�����Լ�ʣ��������Ƶĺ�����m(NaCIO)m(NH3)�ı仯�����ͼ��ʾ����m( NaCIO)��m(NH3)>7.6ʱ��ˮ�����ܵ�ȥ���ʷ����½������ܵ�ԭ����________ ��
���𰸡�4��3 2NH3+ 3NaClO= N2+ 3NaCl+ 3H2O �¶ȹ��ߣ�HClO�����ֽ⣬����ȥ������֮���� �в���NH3��������NO2-��NO3-
��������
��1���÷�Ӧ��NH3��N�ɣ�3�۱�Ϊ0�ۣ����ϼ����ߣ������������ò���Ϊ�������NO2��N�ɣ�4�۱�Ϊ0�ۣ����ϼ۽��ͣ�����ԭ�����ò���Ϊ��ԭ��������������ͻ�ԭ��������ʵ���֮��Ϊ8:6=4:3��
��2���ٸ���ͼʾ�жϷ���������ԭ��Ӧ�ķ�Ӧ���������ݵ�ʧ�����غ��ԭ���غ���д��ѧ����ʽ���¶�Խ�ߣ���ѧ��Ӧ����Խ�죬�����¶ȹ��ߣ�HClO���ȶ��������ֽ⣻
�ڵ�m( NaCIO)��m(NH3)>7.6ʱ��NaCIO�������Խ��Ὣ��������ΪNO3-�ȸ�̬���ʡ�
(1)�÷�Ӧ��NH3��N�ɣ�3�۱�Ϊ0�ۣ����ϼ����ߣ�����������Ӧ������Ϊ�������NO2��N�ɣ�4�۱�Ϊ0�ۣ����ϼ۽��ͣ�������ԭ��Ӧ������Ϊ��ԭ��������������ͻ�ԭ��������ʵ���֮��Ϊ8:6=4:3��
(2)����ͼת�����̿�֪���÷�Ӧ�з�Ӧ��ΪNH3��NaClO��������ΪN2��NaCl2��H2O����˸÷�Ӧ�Ļ�ѧ����ʽΪ��2NH3��3NaClO=N2��3NaCl��3H2O��
���ڷ�Ӧ����������HClO��HClO���ȶ��������ֽ⣬����¶ȹ��ߣ�����ȥ���ʽ��ͣ�
��NaClO���������ԣ���������ʹ�ò���NH3��������NO2-��NO3- �� ʹ��ˮ�����ܵ�ȥ���ʽ��ͣ�

����Ŀ���±��dz����¼��ֳ�������ĵ���ƽ�ⳣ����
���� | ���뷽��ʽ | ����ƽ�ⳣ��K |
CH3COOH | CH3COOH | K=1.6��10-5 |
H2C2O4 | H2C2O4 HC2O4- | K1=5.9��10-2 K2=6.4��10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.4��10-7 K2=5.6��10-11 |
H2S | H2S HS- | K1=9.1��10-8 K2=1.1��10-15 |
�ش��������⣺
(1)ij�¶��£���ˮ�е�c(H+)=2.0��10-7mol��L-1�����¶Ȳ��䣬����ϡ����ʹc(H+)=5.0��10-6mol/L������ˮ�������c(H+)Ϊ___mol��L-1��
(2)�����������ӽ��H+������ǿ����___��
A.HCO3- B.C2O42- C.S2- D.CH3COO-
(3)������1.0mol��L-1��CH3COOH��Һ�е�c(H+)=___mol��L-1��
(4)�����£���ˮϡ��0.1mol��L-1��H2C2O4��Һ������˵����ȷ����___��
A.��Һ��n(H��)��n(OH-)���ֲ���
B.��Һ��ˮ�����c(H��)��c(OH-)���ֲ���
C.��Һ��![]() ���ֲ���
���ֲ���
D.��Һ��c(OH-)����
(5)��CH3COOH��Һ��������Na2CO3��Һ�У���Ӧ�����ӷ���ʽΪ___��
����Ŀ��ij��ѧ��Ӧ�У���Ӧ�����A��B��C�����ʵ���Ũ��(c)��ʱ��(t)��ϵ���±���ʾ��
��ʼ | 2 min | 4 min | 6 min | |
c (A)(mol/L) | 1.45 | 1.28 | 1.00 | 1.00 |
c (B)(mol/L) | 0.38 | 0.72 | 1.28 | 1.28 |
c (C)(mol/L) | 0.095 | 0.18 | 0.32 | 0.32 |
����˵����ȷ���ǣ� ��
A.�÷�Ӧ�Ļ�ѧ����ʽΪA = 2B+C
B.4 minĩA��ת����ԼΪ31%
C.4~6minʱ����Ӧֹͣ��
D.����Ӧ�����ȷ�Ӧ