题目内容
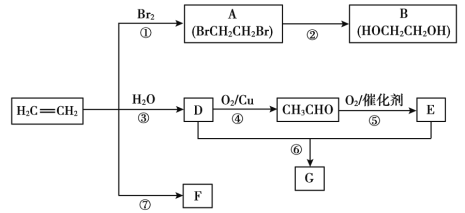
【题目】乙烯是重要有机化工原料。结合以下路线回答:
已知:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
(1)反应①的化学方程式是__。
(2)B的官能团是__。
(3)F是一种高分子,可用于制作食品袋,其结构简式为__。
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,某学习小组在实验室制取乙酸乙酯的主要步骤如下:
i.配制2mL浓硫酸、3mLD(含18O)和2mLE的混合溶液。
ii.按如图连接好装置并加入混合液,用小火均匀加热3~5min。
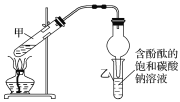
iii.待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
iv.分离出乙酸乙酯,洗涤、干燥。
回答问题:
①装置中球形干燥管,除起冷凝作用外,另一重要作用是___。
②步骤②安装好实验装置,加入药品前还应检查__。
③反应中浓硫酸的作用是__;写出能表示18O位置的制取乙酸乙酯的化学方程式:__。
④上述实验中饱和碳酸钠溶液的作用是__(填字母)。
a.中和乙酸并吸收乙醇
b.中和乙酸和乙醇
c.降低乙酸乙酯的溶解度
d.加速酯的生成,提高其产率
⑤步骤③所观察到的现象是__;从试管乙中分离出乙酸乙酯的实验操作名称是___。
制法二:工业上用CH2=CH2和E直接反应获得G。
a.反应类型是__。
b.与制法一相比,制法二的优点是__。
【答案】H2C=CH2+ Br2→BrCH2CH2Br 羟基(或—OH) ![]() 防止倒吸 装置的气密性 催化剂、吸水剂 CH3COOH+C2H518OH
防止倒吸 装置的气密性 催化剂、吸水剂 CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O ac 试管乙中的液体分成上下两层,上层无色油状,下层液体的红色变浅 分液 加成反应 原子利用率高
CH3CO18OC2H5+H2O ac 试管乙中的液体分成上下两层,上层无色油状,下层液体的红色变浅 分液 加成反应 原子利用率高
【解析】
(1)反应①为H2C=CH2与Br2发生加成反应,生成BrCH2CH2Br。
(2)B的官能团是-OH。
(3)F是一种高分子,可用于制作食品袋,则其为聚乙烯。
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①装置中球形干燥管,除起冷凝作用外,还能防止试管内液体进入反应试管内。
②制取气体时,第一步操作通常为检查装置的气密性。
③反应中浓硫酸的作用是催化剂和吸水剂;乙酸与乙醇发生酯化反应时,酸脱羟基醇脱氢。
④上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇、降低乙酸乙酯的溶解度。
⑤步骤③所得的溶液中,乙酸乙酯与水不互溶,由此可判断反应产生的现象;试管乙中,乙酸乙酯与水分层。
制法二:工业上用CH2=CH2和E直接反应获得G。
a.发生反应为CH2=CH2+CH3COOH→CH3COOCH2CH3,由此可确定反应类型。
b.与制法一相比,制法二中,CH3COOCH2CH3是唯一产物。
(1)反应①为H2C=CH2与Br2发生加成反应,生成BrCH2CH2Br,反应方程式为H2C=CH2+ Br2→BrCH2CH2Br。答案为:H2C=CH2+ Br2→BrCH2CH2Br;
(2)B的官能团是羟基(或-OH)。答案为:羟基(或-OH);
(3)F是一种高分子,可用于制作食品袋,则其为聚乙烯其结构简式为![]() 。答案为:
。答案为:![]() ;
;
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①装置中球形干燥管,除起冷凝作用外,还能防止倒吸。答案为:防止倒吸;
②步骤②安装好实验装置,加入药品前还应检查装置的气密性。答案为:装置的气密性;
③反应中浓硫酸的作用是催化剂和吸水剂;乙酸与乙醇发生酯化反应时,酸脱羟基醇脱氢,反应方程式为CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O。答案为:催化剂、吸水剂;CH3COOH+C2H518OH
CH3CO18OC2H5+H2O。答案为:催化剂、吸水剂;CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;
④上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇、降低乙酸乙酯的溶解度。答案为:ac;
⑤步骤③所得的溶液中,乙酸乙酯与水不互溶,由此可判断反应产生的现象为试管乙中的液体分成上下两层,上层无色油状,下层液体的红色变浅;试管乙中,乙酸乙酯与水分层,采用分液法分离。答案为:试管乙中的液体分成上下两层,上层无色油状,下层液体的红色变浅;分液;
制法二:工业上用CH2=CH2和E直接反应获得G。
a.发生反应为CH2=CH2+CH3COOH→CH3COOCH2CH3,反应类型为加成反应。答案为:加成反应;
b.与制法一相比,制法二中原子利用率高。答案为:原子利用率高。

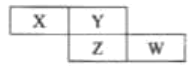
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(1)Y在元素周期表中的位置是___。
(2)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是___。
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为___。
(4)元素X的金属性比元素Y___(填“强”或“弱”),用原子结构的知识解释原因___。
(5)元素Q、元素Z的含量影响钢铁性能,采用如图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。
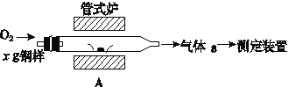
①气体a的成分是__(填化学式)。
②若钢样中元素Z以FeZ的形式存在,在A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是___。
【题目】下表是常温下几种常见弱酸的电离平衡常数:
弱酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | K=1.6×10-5 |
H2C2O4 | H2C2O4 HC2O4- | K1=5.9×10-2 K2=6.4×10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=5.6×10-11 |
H2S | H2S HS- | K1=9.1×10-8 K2=1.1×10-15 |
回答下列问题:
(1)某温度下,纯水中的c(H+)=2.0×10-7mol·L-1,若温度不变,滴入稀硫酸使c(H+)=5.0×10-6mol/L,则由水电离出的c(H+)为___mol·L-1。
(2)下列四种离子结合H+能力最强的是___。
A.HCO3- B.C2O42- C.S2- D.CH3COO-
(3)常温下1.0mol·L-1的CH3COOH溶液中的c(H+)=___mol·L-1。
(4)常温下,加水稀释0.1mol·L-1的H2C2O4溶液,下列说法正确的是___。
A.溶液中n(H+)·n(OH-)保持不变
B.溶液中水电离的c(H+)·c(OH-)保持不变
C.溶液中![]() 保持不变
保持不变
D.溶液中c(OH-)增大
(5)将CH3COOH溶液加入少量Na2CO3溶液中,反应的离子方程式为___。