题目内容
下列说法中正确的是
| A.第3周期的元素中,钠的第一电离能最大 |
| B.最外层都只有一个电子的两原子的性质一定完全相同 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.在同一周期中,随着原子序数的增大,元素的电负性逐渐减小 |
C
解析试题分析:A、金属性越强,第一电离能越小,则第3周期的元素中,钠的第一电离能最小,A不正确;B、最外层都只有一个电子的两原子的性质不一定完全相同,例如氢元素与碱金属元素,B不正确;C、元素电负性越大的原子,非金属性越强,吸引电子的能力越强,C正确;D、在同一周期中,随着原子序数的增大,元素的电负性逐渐增大,D不正确,答案选C。
考点:考查电离能、电负性的有关判断

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列说法正确的是
| A.CO2、CCl4、CH4三个分子中所有原子都满足最外层8电子结构 |
| B.第ⅠA族的金属元素形成的单质的熔点随原子序数的递增而降低 |
| C.第ⅦA族元素形成的单质的熔点随原子序数的递增而降低 |
| D.第ⅠA族元素燃烧形成的氧化物中氧的化合价都不是-2 |
元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
| A.左、下方区域的金属元素 |
| B.金属元素和非金属元素分界线附近的元素 |
| C.右、上方区域的非金属元素 |
| D.稀有气体元素 |
放射性同位素铀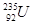 的原子核内的中子数是
的原子核内的中子数是
| A.51 | B.92 | C.143 | D.235 |
电子云是用( )对核外电子运动规律所作的一种描述。
| A.归纳的方法 | B.统计的方法 |
| C.照相法 | D.叠加法 |
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的7/10。则下列说法中不正确的是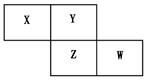
| A.原子半径由大到小排列顺序Z>Y>X |
| B.Y元素的两种同素异形体在常温下都是气体 |
| C.最高价氧化物对应水化物的酸性W>Z |
| D.阴离子半径由大到小排列顺序Z>W>Y |
下列有关说法不正确的是( )
| A.C3H8中碳原子都采用的是sp3杂化 |
| B.O2、CO2、N2都是非极性分子 |
| C.酸性:H2CO3<H3PO4<H2SO4<HClO |
D.CO的一种等电子体为NO+,它的电子式为 |
下列大小关系比较正确的是
| A.离子半径:F-<Na+<Mg2+ | B.电负性:C<O<N |
| C.氢化物的沸点:NH3<PH3<AsH3 | D.碱性: NaOH)>Mg(OH)2> Al(OH)3 |