题目内容
下列有关说法不正确的是( )
| A.C3H8中碳原子都采用的是sp3杂化 |
| B.O2、CO2、N2都是非极性分子 |
| C.酸性:H2CO3<H3PO4<H2SO4<HClO |
D.CO的一种等电子体为NO+,它的电子式为 |
C
解析试题分析:A、C3H8中碳原子全部形成单键,都采用的是sp3杂化,A正确;B、O2、CO2、N2都是非极性分子,B正确;C、次氯酸不是最高价含氧酸,C不正确;D、原子数和价电子数分别都相等的是等电子体,则CO的一种等电子体为NO+,它的电子式为 ,D正确,答案选C。
,D正确,答案选C。
考点:考查杂化轨道、分子极性、含氧酸酸性以及等电子体等

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
下列说法中正确的是
| A.第3周期的元素中,钠的第一电离能最大 |
| B.最外层都只有一个电子的两原子的性质一定完全相同 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.在同一周期中,随着原子序数的增大,元素的电负性逐渐减小 |
下列现象和应用与电子跃迁无关的是( )
| A.激光 | B.焰色反应 | C.原子光谱 | D.石墨导电 |
下列结论错误的是
| A.氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | B.微粒半径:K+>Al3+>S2->Cl— |
| C.酸性:H2SO4>CH3COOH>H2CO3>HClO | D.金属性:K>Ca>Mg>Be |
下列比较或归纳正确的是( )
| A.稳定性:NH3<PH3<ASH3 |
| B.离子半径:Cl->S2->Al3+ |
| C.酸性:HClO4>H2SO4>H3PO4 |
| D.碱性:Be(OH)2>Mg(OH)2>Al(OH)3 |
应用元素周期律和元素周期表,判断下列说法正确的是( )
| A.碱金属单质的熔点随原子序数的增大而降低 |
| B.砹(At)是VIIA族元素,HAt的稳定性大于HCl |
| C.第2周期非金属的气态氢化物溶于水后所得溶液均为酸性 |
| D.铊(TI)与铝同主族,其单质既能与盐酸反应又能与NaOH溶液反应 |
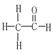 ,其一个分子中存在7对共用电子对
,其一个分子中存在7对共用电子对