题目内容
【题目】ClO2是一种高效、广谱、安全的杀菌、消毒剂,易溶于水。制备方法如下:
(1)步骤Ⅰ:电解食盐水制备氯酸钠。用于电解的食盐水需先除去其中的 Ca2+、Mg2+、SO42-等杂质。在除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的________和NaOH,充分反应后将沉淀一并滤去。
(2)步骤Ⅱ:将步骤Ⅰ得到的食盐水在特定条件下电解得到氯酸钠(NaClO3),再将它与盐酸反应生成ClO2与Cl2,ClO2与Cl2的物质的量比是____________。
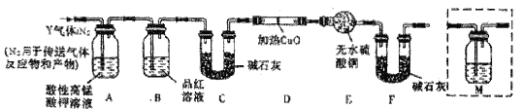
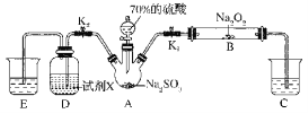
(3)学生拟用左下图所示装置模拟工业制取并收集ClO2,用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得。

反应过程中需要对A容器进行加热,加热的方式为____________;加热需要的玻璃仪器除酒精灯外,还有_________________;
(4)反应后在装置C中可得亚氯酸钠(NaClO2)溶液。已知NaClO2饱和溶液在温度低于38℃时,析出的晶体是NaClO2·3H2O,在温度高于38℃时析出的是NaClO2。根据右上图所示NaClO2的溶解度曲线,请完成从NaClO2溶液中制得NaClO2·3H2O的操作步骤:
①_____________;②_______________;③洗涤;④干燥。
(5)目前我国已成功研制出利用NaClO2制取二氧化氯的新方法,将Cl2通入到NaClO2溶液中。现制取270kg二氧化氯,需要亚氯酸钠的质量是________。
(6)ClO2和Cl2均能将电镀废水中的剧毒CN-氧化为无毒物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的_______倍。
【答案】BaCl2 Na2CO3 2:1 水浴加热 大烧杯、温度计 蒸发浓缩 冷却结晶 362Kg 2.5
【解析】
(1)溶液中的杂质离子为钙离子、镁离子和硫酸根离子,根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀除去,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,所以往粗盐水中先加入过量的BaCl2,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。
(2)电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2与Cl2,再根据化合价升降相等及原子守恒配平,得到离子方程式为2ClO3-+4H++2Cl-=2ClO2+Cl2+2H2O,则ClO2与Cl2的物质的量比是2:1.
(3)ClO2是用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得,所以加热的方式为水浴加热;加热需要的玻璃仪器除酒精灯外,还有大烧杯、温度计;
(4)由溶液制得结晶水合物的基本操作是蒸发浓缩、冷却结晶、洗涤、干燥等。
(5)根据氯气与亚氯酸钠反应的化学方程式和二氧化氯的质量,列出比例式,就可计算出参加反应的亚氯酸钠的质量。设需要亚氯酸钠的质量为x,
2NaClO2+Cl2=2NaCl+2ClO2
181 135
x 270kg 181x=135270kg 解得x=362kg
(6)每摩尔氯气得到2mol电子,每摩尔ClO2得到5mol电子,所以处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的2.5倍。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案