题目内容
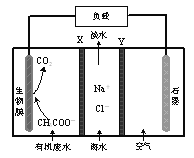
【题目】某微生物脱盐池的装置如图所示,下列说法正确的是
A.电子由石墨电极流出
B.生物膜电极反应式为:CH3COO-+2H2O+8e-=2CO2↑+7H+
C.X、Y依次为阴离子、阳离子选择性交换膜
D.该装置可以将电能转化为化学能
【答案】C
【解析】
由题意和图片装置可知,微生物脱盐池的装置是将废水中有机物CH3COO-的化学能转化为电能的装置,即为原电池,通O2的电极为正极,加入有机废水CH3COO-的电极为负极,正极发生还原反应,负极发生氧化反应,负极反应为CH3COO- + 2H2O-8e- ═ 2CO2↑+7H+,原电池内电路中:阳离子Na+通过阳离子交换膜Y移向正极、阴离子通过阴离子交换膜X移向负极,从而使海水中NaCl含量减少形成淡水,达到脱盐目的,据此分析解答。
A. 通O2的电极为正极,则石墨电极为正极,加入有机废水CH3COO-的电极为负极,则生物膜电极为负极,则电子从生物膜电极流出,A项错误;
B. 生物膜电极为负极,负极发生氧化反应,负极反应式为CH3COO- + 2H2O-8e- ═ 2CO2↑+7H+,B项错误;
C. 在原电池内电路中,阳离子移动向正极,阴离子移动向负极,该装置可使海水中NaCl含量减少形成淡水,达到脱盐目的,则有阳离子Na+通过阳离子交换膜Y移向正极、阴离子Cl-通过阴离子交换膜X移向负极,C项正确;
D. 该装置工作时为原电池,是将化学能转化为电能的装置,D项错误;
答案选C。

【题目】消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1)已知:反应Ⅰ N2(g)+O2(g)=2NO(g) ΔH=a kJ·mol-1
反应Ⅱ 2NO(g)+O2(g)=2NO2(g) ΔH=b kJ·mol-1
反应Ⅲ 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH=c kJ·mol-1
①写出NO2和NH3反应生成N2和液态水的热化学反应方程式______。
②反应Ⅰ中各物质所含化学键键能总和数据如下表,a=______。
物质 | N2 | O2 | NO |
每摩尔物质所含键能总和/kJ·mol-1 | 946 | 498 | 630 |
(2)用次氯酸钠除去氨氮的原理如图所示。该图示的总反应化学方程式为______。

(3)某微生物膜技术能利用电解原理将弱碱性水中的NO![]() 还原为N2,工作原理如图所示。
还原为N2,工作原理如图所示。

①写出阴极的电极反应式:______。
②理论上,若除去0.04 mol NO![]() ,阳极生成气体的体积为______。(标准状况)
,阳极生成气体的体积为______。(标准状况)