题目内容
【题目】臭氧(![]() )在
)在![]() 催化下能将烟气中的
催化下能将烟气中的![]() 、
、![]() 分别氧化为
分别氧化为![]() 和
和![]() ,
,![]() ,也可在其他条件下被还原为
,也可在其他条件下被还原为![]() 。
。
(1)![]() 中心原子轨道的杂化类型为__________;
中心原子轨道的杂化类型为__________;![]() 的空间构型为__________(用文字描述)。
的空间构型为__________(用文字描述)。
(2)与![]() 分子互为等电子体的一种阴离子为__________(填化学式)。
分子互为等电子体的一种阴离子为__________(填化学式)。
(3)![]() 分子中
分子中![]() 键与
键与![]() 键的数目比
键的数目比![]() __________。
__________。
(4)![]() 与
与![]() 反应生成的
反应生成的![]() 中,
中,![]() 以
以![]() 原子与
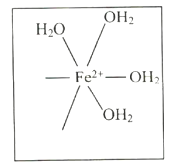
原子与![]() 形成配位键。请在
形成配位键。请在![]() 结构示意图的相应位置补填缺少的配体_________。
结构示意图的相应位置补填缺少的配体_________。
【答案】![]() 平面(正)三角形
平面(正)三角形 ![]() 1:2
1:2 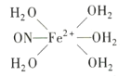
【解析】
(1)![]() 中
中![]() 原子的价层电子对数为4,所以采取
原子的价层电子对数为4,所以采取![]() 杂化。
杂化。![]() 中氮原子上无孤对电子,成键电子对数为3,即
中氮原子上无孤对电子,成键电子对数为3,即![]() 采取
采取![]() 杂化,
杂化,![]() 的空间构型为平面正三角形,故答案为:
的空间构型为平面正三角形,故答案为:![]() ;平面(正)三角形;
;平面(正)三角形;
(2)![]() 与
与![]() 均为3原子、价电子数为18的粒子,故二者互为等电子体,故答案为:
均为3原子、价电子数为18的粒子,故二者互为等电子体,故答案为:![]() ;
;
(3)![]() 分子中含有1个
分子中含有1个![]() 键和2个
键和2个![]() 键,故答案为:1:2;
键,故答案为:1:2;
(4)![]() 中
中![]() 原子与
原子与![]() 形成配位键,故答案为:
形成配位键,故答案为: 。
。

练习册系列答案
相关题目
【题目】恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是( )
A.反应在0~2min内的平均速率为v(SO2)=0.6molL-1min-1
B.反应在2~4min内容器内气体的密度没有变化
C.若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D.保持其他条件不变,起始时向容器中充入1.00molMgSO4和1.00molCO,到达平衡时n(CO2)<0.60mol