题目内容
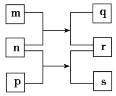
【题目】硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为____。
(2)上述流程中采用稀碱液比用热水更好,理由是___________。
(3)常温下,取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=___mol·L-1。
(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
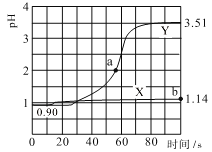
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示)。为使除汞效果最佳,应控制的条件是:x=___,pH控制在___范围。

②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有_____。
(5)常温下利用Fe2+、Fe3+的相互转化,可将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为___________。
【答案】3Na2SO4+8C![]() 3Na2S+4CO2↑+4CO↑ 热水会促进Na2S水解,而稀碱液能抑制Na2S水解 4×10-36 mol·L-1 12 9~10 SO42-、Cl- 2Fe3+ + SO2 + 2H2O=2Fe2+ + SO42- + 4H+
3Na2S+4CO2↑+4CO↑ 热水会促进Na2S水解,而稀碱液能抑制Na2S水解 4×10-36 mol·L-1 12 9~10 SO42-、Cl- 2Fe3+ + SO2 + 2H2O=2Fe2+ + SO42- + 4H+
【解析】
(1)若煅烧所得气体为等物质的量的CO和CO2,则根据原子守恒可知煅烧时发生的总的化学反应方程式为3Na2SO4+8C![]() 3Na2S+4CO2↑+4CO↑。
3Na2S+4CO2↑+4CO↑。
(2)硫化钠是强碱弱酸盐,硫离子水解溶液显碱性,热水会促进Na2S水解,而稀碱液能抑制Na2S水解,所以上述流程中采用稀碱液比用热水更好。
(3)根据硫化铜和氢氧化铜的溶度积常数可知c(Cu2+)·c(S2-)=8.8×10-36、c(Cu2+)·c2(OH-)=2.2×10-20,所以溶液中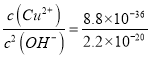 。又因为pH=4,则c(OH-)=1×10-10mol/L,所以溶液中c(S2-)=4×10-36 mol·L-1。
。又因为pH=4,则c(OH-)=1×10-10mol/L,所以溶液中c(S2-)=4×10-36 mol·L-1。
(4)①根据图像可知在pH相等的条件下x=12时汞的去除率最高。而在x值相等的条件下pH在9~10之间时汞的去除率最高。即为使除汞效果最佳,应控制的条件是:x=12,pH控制在9~10范围。
②次氯酸钠与硫化钠的物质的量之比时0.002×2:0.001×1=4:1,次氯酸钠的还原产物是氯化钠,则根据电子得失守恒可知硫化钠的氧化产物是硫酸钠,因此处理后的废水中所含的主要阴离子有SO42-、Cl-。
(5)其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则利用总反应式减去该反应即可得到另一反应的离子方程式为2Fe3+ + SO2 +2H2O=2Fe2+ + SO42- + 4H+。