题目内容
14.下列反应中,在原理上可以设计成原电池的是( )| A. | 氢氧化钙固体与氯化铵固体的反应 | B. | 氨气和氯化氢化合 | ||
| C. | 甲烷与氧气的反应 | D. | 石灰石的分解反应 |
分析 原电池为将化学能转化为电能的装置,所涉及反应为自发进行的氧化反应,以此解答该题.
解答 解:题中只有C为氧化还原反应反应,可设计成原电池反应,其中通入甲烷的电极为负极,通入氧气的电极为正极而A、B、D都不是氧化还原反应,不能设计成原电池.
故选C.
点评 本题考查原电池的设计,注意把握原电池的工作原理以及组成条件,难度不大,注意原电池涉及的反应必须是自发进行的氧化还原反应.

练习册系列答案
相关题目
4.生产生活中处处有化学,下列有关说法错误的是( )
| A. | 铁表面镀锌可增强铁的抗腐蚀性 | |
| B. | 糖类、油脂、蛋白质等是食物中的基本营养物质 | |
| C. | 雾霾、温室效应、光化学烟雾的形成都与氮的氧化物有关 | |
| D. | 氯气和活性炭是常用的漂白剂,但同时使用会降低或失去漂白性 |
5.下列说法错误的是( )
| A. | 红葡萄酒密封窖藏,储存一段时间,香味愈浓,原因之一是储存过程中生成了有香味的酯 | |
| B. | 用浸泡过高锰酸钾溶液的硅土吸收水果或花朵产生的乙烯,可以延迟长水果或花朵的成熟期 | |
| C. | 炒菜时,加一点酒和醋能使菜更加味香可口,原因是有酯类生成 | |
| D. | 油脂能增加食物的滋味,增进食欲,因此在饮食中没有必要控制油脂的摄入量 |
2.填写下表:
| 分子或离子 | SO3 | SO2 | ClO3- | HCN | NF3 | NO3- |
| 中心原子孤电子对数 | 0 | 1 | 1 | 0 | 1 | 0 |
| σ键电子对数 | 3 | 2 | 3 | 2 | 3 | 3 |
| 中心原子的杂化轨道类型 | Sp2 | Sp2 | Sp3 | Sp | Sp3 | Sp2 |
| VSEPR模型名称 | 平面三角形 | V形 | 四面体 | 直线形 | 四面体 | 平面三角形 |
| 分子或离子立体构型名称 | 平面三角形 | V形 | 三角锥 | 直线形 | 三角锥 | 平面三角形 |
19.用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是( )
| A. | CuCl2(CuCl2溶液) | B. | AgNO3(Ag2O) | C. | NaCl(HCl溶液) | D. | CuSO4(Cu(OH)2) |
6.下列物质不属于高分子化合物的是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 淀粉 | D. | 蔗糖 |
3.锌片和铜片用导线连接后插入稀硫酸中可构成原电池,从原电池角度判断锌片作( )
| A. | 正极 | B. | 负极 | C. | 阴极 | D. | 阳极 |
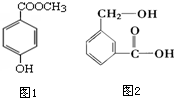 分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途.
分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途.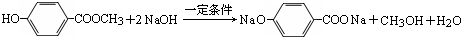 .
.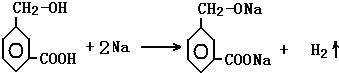 .
.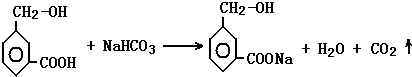 .
.