题目内容
4.现有浓度均为0.1mol/L的下列溶液:①NH4Cl、②CH3COONH4、③NH4HSO4、④氨水(NH3?H2O)、⑤NH4HCO3(1)①溶液显酸性的原因NH4++H2O?NH3•H2O+H+(用离子方程式表示).
(2)已知溶液②呈中性,该溶液中各离子浓度由大到小的顺序是c(CH3COO-)=c(NH4+)>c(H+)=c(OH-).
(3)①、②、③、④四种溶液中c(NH4+)由大到小的顺序是③①②④(填序号).
(4)已知溶液⑤呈碱性,比较②、⑤两溶液的酸碱性,可以得出的结论是HCO3-的水解程度比CH3COO-大或HCO3-比CH3COO-结合H+能力强或CH3COOH酸性比H2CO3强.
分析 (1)氯化铵溶液中,铵根离子水解显示酸性;
(2)CH3COONH4中铵根离子和醋酸根离子的水解程度相当,显示中性,则氢离子和氢氧根离子浓度相等,根据电荷守恒来判断;
(3)根据铵根离子水解平衡移动的影响因素来回答;
(4)醋酸铵显示中性,铵根离子和醋酸根离子的水解程度相当,NH4HCO3溶液呈碱性,则碳酸氢根离子水解程度大于铵根离子的水解程度,据此回答.
解答 解:(1))氯化铵溶液中,铵根离子水解显示酸性,即:NH4++H2O?NH3•H2O+H+,故答案为:NH4++H2O?NH3•H2O+H+;
(2)CH3COONH4中铵根离子和醋酸根离子的水解程度相当,显示中性,则氢离子和氢氧根离子浓度相等,c(H+)=c(OH-),根据电荷守恒,c(CH3COO-)+c(OH-)=c(NH4+)+c(H+),得到:c(CH3COO-)=c(NH4+),所以c(CH3COO-)=c(NH4+)>c(H+)=c(OH-),
故答案为:c(CH3COO-)=c(NH4+)>c(H+)=c(OH-);
(3)①NH4Cl显示酸性,②CH3COONH4显示中性,③NH4HSO4显示酸性,④氨水(NH3?H2O)显示碱性,属于弱碱,电离出的铵根离子浓度最小,硫酸氢铵电离出的氢离子会抑制铵根离子的水解,醋酸根离子会促进铵根离子的水解,所以四种溶液中c(NH4+)由大到小的顺序是③①②④,故答案为:③①②④;
(4)醋酸铵显示中性,铵根离子和醋酸根离子的水解程度相当,NH4HCO3溶液呈碱性,则碳酸氢根离子水解程度大于铵根离子的水解程度,所以HCO3-的水解程度比CH3COO-大或HCO3-比CH3COO-结合H+能力强或CH3COOH酸性比H2CO3强,故答案为:HCO3-的水解程度比CH3COO-大或HCO3-比CH3COO-结合H+能力强或CH3COOH酸性比H2CO3强.
点评 本题考查学生盐的水解原理的应用以及离子浓度大小比较等方面的知识,属于综合知识的考查,难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 乙烯能发生加成反应 | |
| B. | 乙烯易溶于水,也易溶于有机溶剂 | |
| C. | 可用酸性高锰酸钾溶液鉴别乙烯与甲烷 | |
| D. | 乙烯的产量是衡量一个国家石油化工发展水平的标志 |
| A. | 1 L水中含有1 mol MgCl2 | |
| B. | Cl-浓度为2 mol•L-1 | |
| C. | 溶液中含有1 mol MgCl2 | |
| D. | 将95 g MgCl2溶于1 L水中所得的溶液 |
| 牙膏品牌 | 两面针儿童牙膏 | 珍珠防臭牙膏 | 中华透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式,下同);既能与强酸反应又能与强碱反应的是Al(OH)3.
(2)两面针儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(3)从摩擦剂成分考虑,向珍珠防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是有气体生成,该反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(4)中华透明牙膏摩擦剂SiO2是工业制备晶体硅的原料,其反应原理是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑(用化学反应方程式表示).
 .
.
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.

 .写出F与过量NaOH共热时反应的化学方程式
.写出F与过量NaOH共热时反应的化学方程式 .
. 或
或 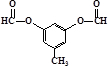 .
.